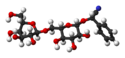
Amigdalina
| |||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C20H27NO11 | ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa | 457,43 g/mol | ||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwne, krystaliczne ciało stałe lub beżowy proszek | ||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||
Amigdalina (z łac. amygdalum – migdał, z gr. αμυγδάλη – migdał) – organiczny związek chemiczny z grupy glikozydów cyjanogennych (syn. nitrylozydów), występujący w nasionach wielu roślin z rodziny różowatych (Rosaceae), głównie migdałowca zwyczajnego (Amygdalus communis), a także pigwy pospolitej (Cydonia oblonga), czeremchy (Padus) i innych drzew owocowych (np. moreli, wiśni, śliw, brzoskwiń). Nadaje nasionom wspomnianych gatunków gorzki smak i specyficzny aromat, zwany w gastronomii migdałowym. W organizmie rozkłada się na glukozę, aldehyd benzoesowy i cyjanowodór. Amigdalinę po raz pierwszy wyodrębnili z gorzkich migdałów w 1830 roku francuscy chemicy Pierre Jean Robiquet i Antoine François Boutron-Charlard[2]. Amigdalinę można wyizolować z nasion migdałów używając rozpuszczalników organicznych[3].
Amigdalina jest toksyczna dla człowieka ze względu na produkty rozkładu, któremu ulega w przewodzie pokarmowym. Związek ten w wyniku działania hydrolazy amigdalinowej ulega hydrolizie do prunazyny, a następnie, pod wpływem hydrolazy prunazynowej, do nitrylu kwasu D-migdałowego i glukozy. Nitryl pod wpływem kolejnego enzymu (liazy) przekształca się w aldehyd benzoesowy i silnie toksyczny cyjanowodór. W efekcie tego procesu spożywanie części roślin zawierających amigdalinę może prowadzić do zatruć[4]. W przypadku podania dożylnego większość związku jest wydalana z moczem (badania na myszach), a część jest metabolizowana do soli cyjanowych, które następnie rodanaza (siarkotransferaza tiosiarczanowa) przekształca do wydalanych z moczem rodanków (tiocyjanianów). Rodanki są również toksyczne, ale w znacznie mniejszym stopniu niż kwas cyjanowodorowy[5][6].
Zastosowania medyczne
W latach 20. XX wieku Ernst Theodore Krebs, Sr. ogłosił teorię, że amigdalina może być skutecznym lekiem na raka, jednak stwierdził, że jest ona zbyt toksyczna do stosowania u ludzi. Koncepcję leczenia raka amigdaliną podjął jego syn, Ernst Theodore Krebs, Jr., opracowując mniej szkodliwą w założeniu pochodną amigdaliny, którą nazwał Laetrile (analizy preparatów handlowych o nazwie Laetrile wykazały jednak, że ich podstawowym składnikiem jest naturalna amigdalina). Z kolei mieszanina amigdaliny i jej formy zmodyfikowanej została określona przez Krebsa jako „witamina B17”. W opisach i specyfikacjach preparatów nazwy te są używane jednak wymiennie[7].
Badania kliniczne nie potwierdziły antynowotworowego działania niewielkich dawek amigdaliny[7][8][9]. Nie stwierdzono zmniejszenia guzów, wydłużenia czasu przeżycia, złagodzenia objawów choroby nowotworowej lub poprawy samopoczucia pacjentów[7]. Zaobserwowano jedynie, w badaniach in vitro, ograniczenie proliferacji i osłabienie zdolności do adhezji niektórych linii komórkowych do śródbłonka naczyń krwionośnych[10][11][12]. Stosowane w badaniu stężenie amigdaliny (10 i więcej mg/ml) było przynajmniej 50 razy wyższe niż dawka uznana za bezpieczną dla człowieka[6]. Powstający podczas metabolizowania podanej doustnie amigdaliny kwas cyjanowodorowy jest silną trucizną i może być przyczyną zatruć[13][9], szczególnie przy jednoczesnym zażywaniu witaminy C[14].
Przypisy
- ↑ a b c (R)-Amygdalin, [w:] PubChem [online], United States National Library of Medicine, CID: 656516 (ang.).
- ↑ A chronology of significant historical developments in the biological sciences. Uniwersytet w Hamburgu, Department of Biology, 2002-08-18. [dostęp 2013-04-12]. (ang.).
- ↑ Andrzej Günther, Amigdalina - jako wstęp do związków naturalnych, „Chemia w Szkole”, ISSN 0411-8634.
- ↑ Paul M. Dewick: Medicinal Natural Products: A Biosynthetic Approach. Wyd. 3. Willey-VCH, 2009, s. 476–477. ISBN 978-0-470-74168-9.
- ↑ Unproven methods of cancer management. Laetrile, „CA: A Cancer Journal for Clinicians”, 41 (3), 1991, s. 187–192, DOI: 10.3322/canjclin.41.3.187, ISSN 0007-9235 [dostęp 2019-07-11].
- ↑ a b Xiaohong Xu, Zuoqing Song, Advanced research on anti-tumor effects of amygdalin, „Journal of Cancer Research and Therapeutics”, 10 (5), 2014, s. 3, DOI: 10.4103/0973-1482.139743, ISSN 0973-1482 [dostęp 2019-07-11].
- ↑ a b c Unproven methods of cancer management. Laetrile, „CA: a cancer journal for clinicians”, 41 (3), 1991, s. 187–192, DOI: 10.3322/canjclin.41.3.187, PMID: 1902140.
- ↑ Barrie R. Cassileth, Gary Deng, Complementary and alternative therapies for cancer, „The Oncologist”, 9 (1), 2004, s. 80–89, DOI: 10.1634/theoncologist.9-1-80, PMID: 14755017.
- ↑ a b Milazzo S, Horneber M. Laetrile treatment for cancer. „Cochrane Database Syst Rev”, s. CD005476, 2015. DOI: 10.1002/14651858.CD005476.pub4. PMID: 25918920.
- ↑ Jasmina Makarević i inni, Amygdalin Influences Bladder Cancer Cell Adhesion and Invasion In Vitro, „PLOS ONE”, 9 (10), 2014, e110244, DOI: 10.1371/journal.pone.0110244, ISSN 1932-6203 [dostęp 2019-07-11].
- ↑ Jasmina Makarević i inni, Amygdalin Blocks Bladder Cancer Cell Growth In Vitro by Diminishing Cyclin A and cdk2, „PLOS ONE”, 9 (8), 2014, e105590, DOI: 10.1371/journal.pone.0105590, ISSN 1932-6203 [dostęp 2019-07-11].
- ↑ Kwon Hee-Young i inni, Apoptosis induction of persicae semen extract in human promyelocytic leukemia (hl-60) cells, „Archives of Pharmacal Research”, 26 (2), 2003, s. 157–161, DOI: 10.1007/bf02976663, ISSN 0253-6269 [dostęp 2019-07-11].
- ↑ Brian O'Brien, Catherine Quigg, Tim Leong, Severe cyanide toxicity from 'vitamin supplements', „European Journal of Emergency Medicine: Official Journal of the European Society for Emergency Medicine”, 12 (5), 2005, s. 257–258, PMID: 16175068.
- ↑ Jonathan Bromley i inni, Life-threatening interaction between complementary medicines: cyanide toxicity following ingestion of amygdalin and vitamin C, „The Annals of Pharmacotherapy”, 39 (9), 2005, s. 1566–1569, DOI: 10.1345/aph.1E634, ISSN 1060-0280, PMID: 16014371 [dostęp 2018-09-14].
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Media użyte na tej stronie
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
The Star of Life, medical symbol used on some ambulances.
Star of Life was designed/created by a National Highway Traffic Safety Administration (US Gov) employee and is thus in the public domain.Structure of Amygdalin; (R)-Amygdaloside; Amigdalina; D(−)-Mandelonitril- β-D-gentiobiosid