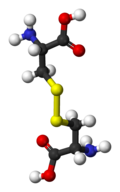
Cystyna
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||
| Wzór sumaryczny | C6H12N2O4S2 | ||||||||||||||||||||||||
| Masa molowa | 240,30 g/mol | ||||||||||||||||||||||||
| Wygląd | biały lub prawie biały, krystaliczny proszek[1] | ||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||
| Numer CAS | 56-89-3 | ||||||||||||||||||||||||
| PubChem | 67678 | ||||||||||||||||||||||||
| DrugBank | DB00138 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||
Cystyna – aminokwas powstały w wyniku połączenia dwóch cząsteczek cysteiny poprzez mostek dwusiarczkowy (jest to więc dimer).
Cystyna uczestniczy w tworzeniu mostków dwusiarczkowych w białkach. Wraz z wiązaniami wodorowymi, siłami van der Waalsa stabilizuje trzeciorzędową strukturę białka.
Przypisy
- ↑ a b c Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b Cystine, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2012-07-17] (ang.).
- ↑ Cystine, [w:] DrugBank [online], University of Alberta, DB00138 (ang.).
Media użyte na tej stronie
Autor: Autor nie został podany w rozpoznawalny automatycznie sposób. Założono, że to MesserWoland (w oparciu o szablon praw autorskich)., Licencja: CC-BY-SA-3.0
Ball-and-stick model of cystine