Deuteron
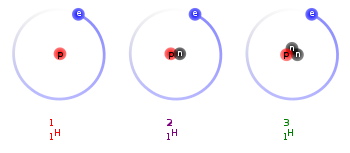
Deuteron – jądro atomowe deuteru, czyli izotopu wodoru 21H, zwanego ciężkim wodorem. Deuteron składa się z jednego neutronu i jednego protonu.
Liczba atomowa deuteronu wynosi Z=1, zaś liczba masowa A=2, energia wiązania 2,225 MeV[1]. Deuteron oznaczany jest symbolem chemicznym D, lub częściej symbolem d, przyjętym w zapisach przemian jądrowych.
Deuterony są wykorzystywane do wywoływania reakcji jądrowych, a następnie do produkcji nuklidów promieniotwórczych, najczęściej w reakcji jądrowej z emisją neutronu (niektóre z nich są ważnym źródłem prędkich neutronów) tzw. reakcje (d,n). Reakcje te cechuje duża wydajność. Deuterony stosowane są także do badania sił jądrowych (jest to najprostszy układ jądrowy, którego składniki mogą posiadać moment pędu związany z ruchem obrotowym).
Deuterony występują w przyrodzie we wnętrzach gwiazd, gdzie są jednym z elementów łańcucha przemian termojądrowych cyklu protonowego.
Pierwsza antycząstka deuteronu, antydeuteron, została wytworzona i zaobserwowana przez naukowców ze Stanów Zjednoczonych. Był to pierwszy przypadek wytworzenia antymaterii (a nie pojedynczych antycząstek).
Zobacz też
Przypisy
- ↑ deuteron, [w:] Encyklopedia PWN [online] [dostęp 2022-09-16].
Bibliografia
- Ryszard Szepke: 1000 słów o atomie i technice jądrowej. Wydawnictwo Ministerstwa Obrony Narodowej, 1982. ISBN 83-11-06723-6. (pol.)
Linki zewnętrzne
Media użyte na tej stronie
Autor:
- derivative work: Uvainio (talk)
- Hydrogen_Deuterium_Tritium_Nuclei_Schmatic-ja.svg: Dirk Hünniger, translated by user:was a bee
The three isotopes of hydrogen.