Elektroda wodorowa
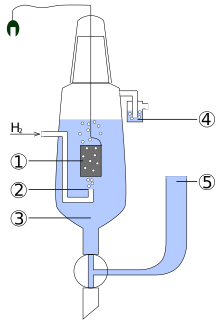
1 – elektroda platynowa
2 – bełkotka uwalniająca pęcherzyki wodoru
3 – roztwór kwasu
4 – płuczka blokująca dostęp tlenu
5 – zbiornik z zapasem elektrolitu
Elektroda wodorowa (SHE, z ang. standard hydrogen electrode) – w elektrochemii, gazowa elektroda redoks (półogniwo wodorowe), wykonana z platyny pokrytej czernią platynową i – po umieszczeniu w kwaśnym elektrolicie – omywana gazowym wodorem. Gdy ciśnienie cząstkowe wodoru wynosi 101,325 kPa, a jony wodorowe w roztworze mają aktywność jednostkową, uzyskiwany jest potencjał standardowy E0, który przyjęto umownie jako zerowy (we wszystkich temperaturach)[1][2].
Elektroda wodorowa jest punktem odniesienia potencjału w elektrochemii. Odniesienie potencjału metalu do elektrody wodorowej jako standardu wynika między innymi ze sposobu reakcji metali z kwasami.
Wyróżnia się standardową elektrodę wodorową (SEW) pracującą w warunkach standardowych i normalną elektrodę wodorową (NEW) pracującą w warunkach normalnych. Czasem również wyróżnia się odwracalną elektrodę wodorową (gdy pH ≠ 0 lub ciśnienie gazowego wodoru ≠ 100 kPa).
Potencjał absolutny standardowej elektrody wodorowej oszacowany jest na 4,44 ± 0,02 V (w 25 °C)[1].
Powtarzalność i interferencje
Elektroda wodorowa cechuje się znakomitą powtarzalnością (bias mniejszy niż 10 μV przy porównaniu potencjału dwóch dobrze wykonanych elektrod wodorowych[3]).
Ze względu na adsorpcję ważne jest chronienie powierzchni elektrody i elektrolitu przed substancjami organicznymi i tlenem atmosferycznym. Nieorganicznych jonów, które mogą się redukować, również należy unikać (np. Fe3+, CrO42-).
Kationy redukujące się i osadzające się na elektrodzie również mogą być źródłem błędów w działaniu elektrody: srebro, rtęć, miedź, ołów, kadm i tal.
Substancje, które mogą zdezaktywować („zatruć”) punkty katalityczne na powierzchni elektrody wodorowej, to arsen, siarczki i inne związki siarki, substancje koloidalne, alkaloidy i materiały spotykane w organizmach żywych[4].
Zobacz też
Przypisy
- ↑ a b Standard hydrogen electrode, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.S05917, ISBN 0-9678550-9-8 (ang.).
- ↑ elektroda wodorowa, [w:] Encyklopedia PWN [online] [dostęp 2012-10-10].
- ↑ D.T. Sawyer, A. Sobkowiak, J.L. Roberts, Jr., Electrochemistry for Chemists, 2nd edition, John Wiley and Sons, Inc., 1995.
- ↑ D.J.G. Ives, G.J. Janz, Reference Electrodes. Theory and Practice, Academic Press, 1961.
Media użyte na tej stronie
Autor:
- Standard_hydrogen_electrode.jpg: Kaverin
- derivative work: Henry Muelpfordt (talk)
Standard hydrogen electrode scheme:
- platinized platinum electrode
- hydrogen gas
- acid solution with an activity of H+=1 mol/l
- hydroseal for prevention of oxygen inteference
- reservoir via which the second half-element of the galvanic cell should be attached
