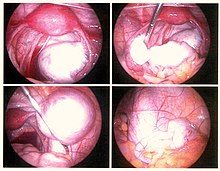
Endometrioza
| Endometriosis | |
| ICD-10 | |
|---|---|
| N80.0 | Gruczolistość macicy |
| N80.1 | Gruczolistość śródmaciczna jajnika |
| N80.2 | Gruczolistość śródmaciczna jajowodu |
| N80.3 | Gruczolistość śródmaciczna otrzewnej miednicy mniejszej |
| N80.4 | Gruczolistość śródmaciczna przegrody odbytniczo-pochwowej i pochwy |
| N80.5 | Gruczolistość śródmaciczna jelita |
| N80.6 | Gruczolistość śródmaciczna w bliźnie skórnej |
| N80.8 | Inna gruczolistość śródmaciczna o innej lokalizacji |
| N80.9 | Gruczolistość śródmaciczna, nie określona |
| DiseasesDB | |
| OMIM | |
| MedlinePlus | |
| MeSH | |
Endometrioza, gruczolistość zewnętrzna – obecność błony śluzowej macicy (endometrium) poza jamą macicy[1]. Ognisko endometriozy zawiera komórki gruczołowe i zrąb endometrium[1]. Choroba najczęściej dotyczy kobiet w wieku rozrodczym.
Historia
Chorobę opisał jako pierwszy Daniel Shroen w 1690 w dziele Disputatio Inauguralis Medica de Ulceribus Ulceri[2]. Objawy dokładnie przedstawił Arthur Duff w 1769.
Począwszy od XIX wieku wysuwano hipotezy dotyczące patogenezy endometriozy. Friedrich Daniel von Recklinghausen przypuszczał, że tkanka endometrialna pochodzi z przewodów Wolffa. Thomas Stephen Cullen upatrywał jej źródła w pozostałościach przewodów Müllera. Heinrich Wilhelm Waldeyer jako pierwszy wysunął teorię metaplazji w 1870 roku. Iwanhofen w 1898 wysunął przypuszczenie, że powstaje ona z metaplazji nabłonka otrzewnej. Meyer w 1903 uważał, że metaplazji sprzyjać miałoby wpuklanie się nabłonka w podścielisko, pod wpływem czynników hormonalnych i zapalnych.
Kolejne hipotezy wysunęli: Pick w 1905, Halban w 1924, Navrital i Kramer w 1936, a John Sampson w 1925 roku – hipotezę „miesiączkowania wstecznego”.
W 1980 Weed i Arquembourg zaproponowali, że przyczyną choroby jest niewydolność układu immunologicznego wywodzącego się z przewodów Müllera[3]. Dwa lata później Malick uznał, że u podłoża endometriozy leży wrodzona lub nabyta osłabiona aktywność fibrynolityczna otrzewnej.
Patogeneza choroby wciąż budzi duże kontrowersje; powszechność łagodnych postaci endometriozy Johannes Evers uznał za podstawę do twierdzenia, że "endometrioza nie istnieje"[4]
Epidemiologia
Ocenia się, że endometrioza występuje u 7–15% miesiączkujących kobiet[5]. Rzadko występuje w okresie pomenopauzalnym oraz przed menarche[6]. Opisano pojedyncze przypadki na świecie występowania endometriozy u mężczyzn leczonych hormonalnie z powodu raka gruczołu krokowego[7].
Patogeneza
Ogniska endometriozy usytuowane są najczęściej wewnątrz jamy otrzewnej (w 94–97% przypadków) lub znacznie rzadziej poza nią (szyjka macicy, sklepienie pochwy, srom, pęcherz moczowy lub okolica pachwinowo-udowa). Powstają guzki, zrosty i torbiele czekoladowe. Patomechanizm jest różny w zależności od miejsca występowania „dodatkowej” tkanki. Teorie wyjaśniające:
- regurgitacja, inaczej „wsteczna menstruacja” (teoria Sampsona z 1927) – wydostanie się komórek endometrium do jamy otrzewnej poprzez jajowód. Być może u wielu kobiet dochodzi do wstecznego przepływu w czasie menstruacji, ale ich układ odpornościowy jest w stanie uprzątnąć komórki i zapobiec implantacji,
- implantacja (fizjologia) – rozprzestrzenianie się endometriozy bezpośrednio. Przeniesienie endometrium poza jamę macicy może nastąpić w trakcie porodu cesarskiego, w przypadku operacji laparoskopowych, a także po nacięciu krocza do blizn,
- metaplazja komórek wyściółki otrzewnej,
- rozsiew – w rzadkich przypadkach endometrioza może być przeniesiona drogą naczyń krwionośnych i limfatycznych do odległych narządów (płuca, mózg, kości).
- toksyny w środowisku - w badaniach laboratoryjnych ludzkie tkanki endometrium wystawione na działanie dioksyn (i związków dioksynopodobnycj) i Polichlorowane bifenyle stawały się oporne na progesteron i podatne na zapalenie. Brak progesteronu powodował brak wyciszenia enzymów Metaloproteinazy macierzy pozakomórkowej, przez co tkanka endometrium stawała się bardziej inwazyjna[8]
W powstawaniu endometriozy ma znaczenie nadmiar estrogenów oraz czynniki genetyczne (dziedziczne) – córki lub siostry pacjentek z endometriozą mają większe prawdopodobieństwo rozwinięcia endometriozy. W 2005 powiązano występowanie endometriozy z locus 10q26[9]
Ryzyko endometriozy zmniejsza karmienie piersią. Każde trzy miesiące karmienia wyłącznie piersią zmniejszają ryzyko rozwoju o 14% w porównaniu do kobiet karmiących piersią tylko przez miesiąc[10].
Objawy i przebieg
Choroba rozwija się powoli, a przebiega często ze skąpymi objawami chorobowymi lub bezobjawowo. Zaczyna zwracać uwagę chorej z uwagi na ból podczas współżycia, problemy z zajściem w ciążę.
Endometrioza objawia się dolegliwościami bólowymi w miednicy mniejszej, zaburzeniami cyklu miesięcznego oraz obfitymi krwawieniami miesiączkowymi, często występuje PMS. Bardzo często doprowadza do niedrożności jajowodów i zaburzenia zdolności rozrodczych bądź do bezpłodności.
Rzadszymi objawami są plamienia lub krwawienia acykliczne, nadmierne krwawienia miesięczne (typowo w adenomyosis), krwiomocz (postać pęcherzowa), krwawienia z przewodu pokarmowego (postać jelitowa), plamienia kontaktowe (lokalizacja szyjkowa).
Niekiedy objawem endometriozy jest nawracająca odma opłucnowa charakteryzująca się bólem klatki piersiowej i dusznością[11][12].
Według Global Study of Women's Health z 2011 roku, dolegliwości związane z endometriozą zmniejszają wydajność pracujących kobiet nawet o 11 godzin w 40 godzinnym tygodniu pracy.
Podział Martiusa wyróżnia trzy kliniczne postacie endometriozy:
- endometriosis genitalis interna – w mięśniu macicy lub jajowodzie
- endometriosis genitalis externa – w innych miejscach układu płciowego
- endometriosis extragenitalis – poza układem płciowym.
Skutki nieleczonej endometriozy
- Silne bóle,
- Stany depresyjne,
- Problemy ze współżyciem seksualnym,
- Obniżenie płodności bądź niepłodność,
- Zaburzenia jelita i pęcherza.
Rozpoznanie
Najczęściej za pomocą laparoskopii lub w czasie laparotomii z biopsją. Mniej precyzyjną metodą jest punkcja zatoki Douglasa i zaaspirowanie z niej krwi (kuldocenteza), co przed laty było istotnym kryterium rozpoznania. Stosowane są także nieinwazyjne metody diagnostyczne USG i MRI. Niestwierdzenie ognisk endometriozy w tych badaniach nie wyklucza choroby, ponieważ niekiedy są one zbyt małe lub w ten sposób umiejscowione, że jest to niemożliwe. U wielu kobiet z endometriozą podniesiony jest poziom CA 125, który jest nieswoistym markerem[13].
Leczenie
Nie jest znana dokładna przyczyna tej choroby i z tego powodu leczenie ma charakter objawowy. Leczenie polega na podawaniu leków z grupy gestagenów, leków hamujących wydzielanie gonadotropin (np. danazol) lub analogów gonadoliberyny co ma na celu zahamowanie podziałów komórkowych endometrium, głównie poprzez zmniejszenie poziomu estrogenów. Pod wpływem gestagenów przerośnięte obszary śluzówki macicy, które są zmianami o charakterze ogniskowym są mniej skłonne do krwawień. Jeśli leczenie za pomocą gestagenów nie przynosi efektów, należy zastosować leczenie operacyjne, polegające na wycięciu zmian ogniskowych. Jednak nie usuwa to przyczyn choroby, która tworzy nowe ogniska i zrosty. W ciężkich przypadkach stosuje się usunięcie jajników, zwykle już zniszczonych przez torbiele czekoladowe i zrosty. Dawniej stosowano też leczenie androgenami, obecnie się tej metody nie stosuje. Przyjmowanie tabletek antykoncepcyjnych zmniejsza ból miesiączkowy związany z endometriozą[14]. Celem leczenia operacyjnego jest też możliwe usunięcie zrostów, i uruchomieniu narządów miednicy mniejszej, co zmniejsza objawy bólowe u chorej.
Leczenie chirurgiczne
- usunięcie ognisk i torbieli endometrialnych techniką laparotomii lub laparoskopii
- biopsja - obecnie niezalecana
- laparoskopia lub laparotomia zwiadowcza
- usunięcie macicy z, zachowaniem lub nie, przydatków
Leczenie farmakologiczne
- dienogest
- danazol
- analogi gonadoliberyny (aGnRH)
- progestageny
- preparaty estrogenowo-progestagenowe
- wkładka wewnątrzmaciczna uwalniająca lewonorgestrel
- inhibitory aromatazy
- selektywne modulatory receptorów progesteronu
Leczenie skojarzeniowe (połączenie leczenia chirurgicznego z leczeniem farmakologicznym w celu zachowania zdolności rozrodczych)
Przypisy
- ↑ a b Grzegorz H. Bręborowicz (red.), Położnictwo i ginekologia, Warszawa: Wydawnictwo Lekarskie PZWL, 2006, ISBN 83-200-3443-4.
- ↑ Sutton C. The history of endometriosis. [w:] Modern Management of Endometriosis. CRC Press, 2005 s. 1-17 ISBN 1-84214-276-3
- ↑ JC Weed, PC Arquembourg. Endometriosis: can it produce an autoimmune response resulting in infertility?. „Clinical obstetrics and gynecology”. 23 (3), s. 885-93, Sep 1980. PMID: 7418287.
- ↑ Johannes L.H. Evers, Endometriosis does not exist; all women have endometriosis, „Human reproduction (Oxford, England)”, 9 (12), 1994, s. 2206-9, DOI: 10.1093/oxfordjournals.humrep.a138421, PMID: 7714129.
- ↑ Bręborowicz, Położnictwo i ginekologia s. 875
- ↑ Ronald E Batt, Mohamed F.M Mitwally, Endometriosis from thelarche to midteens: pathogenesis and prognosis, prevention and pedagogy, „Journal of pediatric and adolescent gynecology”, 16 (6), 2003, s. 337–47, DOI: 10.1016/j.jpag.2003.09.008, PMID: 14642954.
- ↑ Martin JD, Hauck AE. Endometriosis in the male.. „The American surgeon”. 7 (51), s. 426–30, lipiec 1985. PMID: 4014886.
- ↑ Kaylon L. Bruner-Tran, Kevin G. Osteen, Dioxin-like PCBs and endometriosis, „Systems Biology in Reproductive Medicine”, 2, 56, 2010, s. 132-146, DOI: 10.3109/19396360903381023, PMID: 20377312, PMCID: PMC2867352 (ang.).
- ↑ Treloar SA. i inni, Genomewide linkage study in 1,176 affected sister pair families identifies a significant susceptibility locus for endometriosis on chromosome 10q26., „American journal of human genetics”, 77 (3), 2005, s. 365–76, DOI: 10.1086/432960, PMID: 16080113, PMCID: PMC1226203.
- ↑ Leslie V Farland i inni, History of breast feeding and risk of incident endometriosis: prospective cohort study, „British Medical Journal”, 358, BMJ Publishing Group Ltd, 2017, DOI: 10.1136/bmj.j3778, PMID: 28851765, PMCID: PMC5574033 (ang.).
- ↑ Avni K.P. Skandhan, Thoracic endometriosis | Radiology Reference Article | Radiopaedia.org, Radiopaedia [dostęp 2021-02-22] (ang.).
- ↑ Lisa Sanders, The Woman Was Fit and Healthy. Why Did Her Lung Mysteriously Collapse? (Published 2018), „The New York Times”, 28 marca 2018, ISSN 0362-4331 [dostęp 2021-02-22] (ang.).
- ↑ Amaral VF. i inni, Positive correlation between serum and peritoneal fluid CA-125 levels in women with pelvic endometriosis., „São Paulo medical journal = Revista paulista de medicina”, 124 (4), 2006, s. 223–7, DOI: 10.1590/s1516-31802006000400010, PMID: 17086305.
- ↑ Tasuku Harada i inni, Low-dose oral contraceptive pill for dysmenorrhea associated with endometriosis: a placebo-controlled, double-blind, randomized trial., „Fertility and sterility”, 90 (5), 2008, s. 1583–8, DOI: 10.1016/j.fertnstert.2007.08.051, PMID: 18164001.
Bibliografia
- Grzegorz H Bręborowicz, Beata Banaszewska: Położnictwo i ginekologia. T. 2, Ginekologia. Warszawa: Wydawnictwo Lekarskie PZWL, 2007, s. 875–886. ISBN 978-83-200-3541-4 (t. 2).
- Antoni Palatyński: Endometrioza. Warszawa: Państwowy Zakład Wydawnictw Lekarskich, 1990. ISBN 83-200-1434-4.
Linki zewnętrzne
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Media użyte na tej stronie
The Star of Life, medical symbol used on some ambulances.
Star of Life was designed/created by a National Highway Traffic Safety Administration (US Gov) employee and is thus in the public domain.endometriosis of the peritoneum
endometriotic lesions in the Douglas pouch and on the right sacrouterine ligament
perforated endometriosis cyst of the left ovary