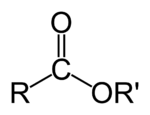
Estry
Estry (od niem. Essigäther – octan etylu, Essig – ocet i Äther – eter[1]) – grupa organicznych związków chemicznych będących produktami kondensacji kwasów i alkoholi lub fenoli. Komponentami kwasowymi mogą być zarówno kwasy karboksylowe, jak i kwasy nieorganiczne.
Bezpośrednia reakcja między kwasem karboksylowym i alkoholem nazywa się estryfikacją. Reakcja ta jest odwracalna, zachodzi w środowisku kwaśnym.
- R1
COOH + R2
OH ⇄ R1
COOR2
+ H
2O
Równowagę tej reakcji można przesunąć w prawo (w kierunku tworzenia estru) przez usuwanie jednego z produktów, wody lub estru, ze środowiska reakcji, np. przez destylację lub zastosowanie dodatkowego reagenta konsumującego wodę.
Estry niższych kwasów karboksylowych i alkoholi alifatycznych o krótkich łańcuchach węglowych są cieczami słabo mieszającymi się z wodą, o intensywnym i dość przyjemnym zapachu. Są one jednak w większych dawkach toksyczne, a niektóre są też rakotwórcze. Estry te są stosowane jako rozpuszczalniki organiczne o średniej polarności.
Estry kwasów karboksylowych z długimi grupami alkilowymi, czyli zawierające wyższe kwasy tłuszczowe lub wyższe alkohole alifatyczne, są głównymi składnikami wosku naturalnego. Z kolei estry wyższych kwasów tłuszczowych i gliceryny to tłuszcze.
W organizmach żywych poza licznymi estrami kwasów karboksylowych, powszechnie występują estry kwasu fosforowego, np. nukleotydy i kwasy nukleinowe (DNA, RNA). Estry kwasu azotowego są często nietrwałe i mogą mieć właściwości wybuchowe, np. nitroceluloza i nitrogliceryna.
Otrzymywanie
Estry powstają np. w reakcji alkoholi z kwasami, chlorkami kwasowymi, bezwodnikami kwasowymi i innymi pochodnymi kwasów. Estry można też otrzymać z innych estrów w reakcji transestryfikacji, tj. wymiany reszty alkoholowej estru wyjściowego.
Właściwości fizyczne
Estry niższych kwasów karboksylowych i alkoholi są cieczami trudno rozpuszczalnymi w wodzie, o intensywnym i dość przyjemnym zapachu, toksyczne w większych dawkach. W miarę wzrostu długości łańcucha zmienia się ich stan skupienia od cieczy, przez gęste oleiste płyny, do ciał stałych. Estry wyższych kwasów są bezwonne i nierozpuszczalne w wodzie. Estry kwasów tłuszczowych i gliceryny to tłuszcze. Temperatury topnienia i wrzenia estrów są niższe niż odpowiednich kwasów karboksylowych. Przyczyną tej różnicy jest fakt, że cząsteczki estrów nie zawierają grupy −OH i nie mogą tworzyć wiązań wodorowych między sobą. W wodzie rozpuszczają się jedynie estry o niskich masach molowych (dzięki tworzeniu wiązań wodorowych między –COO– a cząsteczkami wody). Są dobrymi rozpuszczalnikami dla związków organicznych.
Właściwości chemiczne
Estry w wodzie ulegają hydrolizie (dla estrów kwasów karboksylowych reakcja ta bywa nazywana zmydlaniem) z różną szybkością, zależną od budowy estru. Reakcja ta może być katalizowana zarówno przez kwasy, jak i zasady.
Zapach estrów
Wiele estrów kwasów karboksylowych wykazuje intensywny, przyjemny zapach. Najliczniejszą grupą tego rodzaju estrów są pochodne kwasu octowego i kwasu masłowego:
Octan izoamylu (zapach bananów)
Lista zapachów wybranych estrów
| Ta sekcja od 2019-04 wymaga zweryfikowania podanych informacji. |
| heksanian allilu | ananas |
| octan benzylu | gruszka, truskawka, jaśmin |
| octan bornylu | sosna aromat drzewa |
| maślan butylu | ananas |
| maślan etylu | ananas |
| octan etylu | brzoskwinia, ananas, malina |
| butanian etylu | banan, ananas, truskawka |
| heksanian etylu | truskawka |
| cynamonian etylu | cynamon |
| mrówczan etylu | cytryna, rum, truskawka |
| heptanian etylu | morela, wiśnia, winogrono, malina |
| izowalerian etylu | jabłko |
| mleczan etylu | winogrono |
| nonanian etylu | winogrono |
| walerian etylu | jabłko |
| octan geranylu | geranium |
| butanian geranylu | wiśnia |
| pentanian geranylu | jabłko |
| octan izobutylu | wiśnia, malina, truskawka |
| mrówczan izobutylu | malina |
| octan izopentylu | gruszka, banan |
| octan linalolu | lawenda, szałwia |
| butanian linalolu | brzoskwinia |
| mrówczan linalolu | jabłko, brzoskwinia |
| octan mentolu | mięta pieprzowa |
| antranilan metylu | winogrono, jaśmin |
| benzoesan metylu | owocowy, jagodlin |
| octan metylobenzylu | wiśnia |
| butanian metylu | ananas, jabłko |
| cynamonian metylu | truskawka |
| pentanian metylu | kwiatowy |
| octan metylofenylu | miód |
| salicylan metylu | piwo korzenne, krzew zimozielny |
| kaprylan nonylu | pomarańcza |
| octan oktylu | owocowy-pomarańcza |
| butanian oktylu | pasternak |
| octan pentylu | jabłko, banan |
| butanian pentylu | morela, gruszka, ananas |
| heksanian pentylu | jabłko, ananas |
| pentanian pentylu | jabłko |
| izobutanian propylu | rum |
| octan n-butylu | banan |
| butanian terpylu | wiśnia |
Zobacz też
- acydoliza
- ortoestry
Przypisy
Media użyte na tej stronie
Redirect arrow, to be used in redirected articles in Wikipedias written from left to right. Without text.
Structure of benzyl acetate
Structure of butyl butyrate
Essigsäureoctylester
Autor: Trengarasu, Licencja: CC BY-SA 3.0
Phosphate Functional Group Chemical Structure