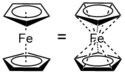
Ferrocen
| |||||||||||||||||||||||||||||||||||||||||||
 Próbka ferrocenu | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C10H10Fe | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | Fe(C5H5)2 | ||||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 186,03 g/mol | ||||||||||||||||||||||||||||||||||||||||||
| Wygląd | czerwonopomarańczowe kryształy[1] o zapachu podobnym do kamfory[2] | ||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 102-54-5 | ||||||||||||||||||||||||||||||||||||||||||
| PubChem | 11985121 | ||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||
Ferrocen – metaloorganiczny związek chemiczny, aromatyczny kompleks sandwiczowy należący do grupy metalocenów[5][6][7], w którym atom żelaza (formalnie na II stopniu utlenienia, w rzeczywistości na zerowym) tworząc atom centralny znajduje się między dwoma płaskimi, równolegle ułożonymi pierścieniami cyklopentadienylowymi. Ferrocen należy do grupy π kompleksów.
Budowa cząsteczki
W strukturze budowy ferrocenu występuje specyficzny rodzaj wiązań chemicznych. Jest wiązanie polegające na uwspólnieniu po jednym elektronie π z każdego atomu węgla w pierścieniu cyklopentadienylowym z centralnym atomem żelaza. W rezultacie powstaje układ 10 wiązań chemicznych, z których każde jest bardzo słabe, ale łącznie generuje to bardzo silne oddziaływanie, na skutek czego ferrocen jest bardzo trwałym i stabilnym kompleksem.
Mimo iż formalnie atom żelaza w ferrocenie jest na II stopniu utlenienia, w rzeczywistości własności ferrocenu w stanie podstawowym, a także badania rentgenograficzne wskazują na to, że ma on raczej cechy kompleksu na zerowym stopniu utlenienia.
Właściwości
Jest to substancja stała o barwie czerwonopomarańczowej, tworzy kryształy o barwie brązowopomarańczowej. Nierozpuszczalny w wodzie, trudno rozpuszczalny w rozpuszczalnikach organicznych np. benzenie i eterze. Temperatura topnienia ok. 173-174 °C, temperatura wrzenia 249 °C. Jest bardzo trwały termicznie. Wykazuje niektóre właściwości związków aromatycznych. Ferrocen ulega reakcjom acylowania i alkilowania metodą Friedla-Craftsa, jest o wiele bardziej reaktywny w tych reakcjach niż benzen.
Ferrocen jest łatwo utlenić elektrochemicznie, na skutek czego powstaje jego utleniona forma – jon ferroceniowy. Jest to proces odwracalny. Jon ten jest również bardzo stabilny, niemal tak samo jak sam ferrocen. Wynika to z faktu, że oderwanie jednego elektronu z ferrocenu nie powoduje prawie żadnej zmiany w geometrii jego struktury. Dzięki temu ferrocen jest bardzo wdzięcznym obiektem do badania mechanizmów reakcji redoks.
Zastosowanie
Ferrocen posiada szereg zastosowań. Jest stosowany jako dodatek do paliw. W olejach napędowych pełni on rolę środka zapobiegającego osadzaniu się sadzy w układzie wydechowym. Mieszaniny pochodnych ferrocenu stosuje się też w USA jako zamiennik tetraetyloołowiu w benzynach do samochodów na benzynę „ołowiową”.
Historia
Ferrocen był pierwszym, otrzymanym kompleksem cyklopentadienylowym. Został otrzymany przez przypadek w 1951 r., równolegle w kilku laboratoriach, w bezpośredniej reakcji pyłu żelaza z cyklopentadienem, w ramach której chciano doprowadzić do otwarcia pierścienia cyklopentadienowego. Zamiast tego otrzymywano niezmiennie pomarańczowe kryształy, o strukturze których trwały liczne dyskusje, aż do roku 1954, kiedy to badania rentgenograficzne, NMR i IR przekonały chemików o kanapkowej budowie tego związku. Ze względu na to, że taka struktura stała w sprzeczności z obowiązującą wówczas teorią wiązań chemicznych, aż do połowy lat 70. trwały badania i dyskusje nad naturą elektronową tego związku, które przy okazji doprowadziły do rozwoju chemii metaloorganicznej.
Za badania w tej dziedzinie Ernst Fischer i Geoffrey Wilkinson otrzymali Nagrodę Nobla w dziedzinie chemii w 1973 r.
Przypisy
- ↑ a b c d Podręczny słownik chemiczny, Romuald Hassa (red.), Janusz Mrzigod (red.), Janusz Nowakowski (red.), Katowice: Videograf II, 2004, s. 131, ISBN 83-7183-240-0.
- ↑ a b c d e Ferrocen (ang.). The Chemical Database. Wydział Chemii Uniwersytetu w Akronie. [dostęp 2012-08-17].[niewiarygodne źródło?]
- ↑ a b Ferrocene, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2012-08-17] (ang.).
- ↑ a b Ferrocen (nr F408) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Polski.
- ↑ Michael B. Smith, Jerry March: March's Advanced Organic Chemistry.Reactions, Mechanisms and Structure. Wyd. 6. Wiley, 2007, s. 66. ISBN 978-0-471-72091-1.
- ↑ sandwich compounds, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.S05468, ISBN 0-9678550-9-8 (ang.).
- ↑ metallocenes, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.M03865, ISBN 0-9678550-9-8 (ang.).
Bibliografia
- Wilkinson, Geoffrey. The iron sandwich. A recollection of the first four months. „Journal of Organometallic Chemistry”. 100 (1), s. 273-278, 1975. DOI: 10.1016/S0022-328X(00)88947-0 (ang.).
Media użyte na tej stronie
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
A photo of ferrocene in a powdered form.
The hazard symbol for flammable/highly flammable substances according to directive 67/548/EWG by the European Chemicals Bureau.
Autor: Episodesn, Licencja: CC BY-SA 3.0
Ferrocene organometallic sandwich complex
Dwie prezentacje wiązań w ferrocenie