Hydroksyloamina
| |||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | H3NO | ||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | NH2OH | ||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 33,03 g/mol | ||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | białe płatki lub igły[2] | ||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||
Hydroksyloamina – nieorganiczny związek chemiczny, pochodna amoniaku, w której jeden atom wodoru został zastąpiony grupą hydroksylową. Najprostsza hydroksyamina.
Jest to bezbarwne higroskopijne, krystaliczne ciało stałe o temperaturze topnienia wynoszącej 33,1 °C. Jest silnie trująca, podczas ogrzewania rozkłada się z wydzieleniem ciepła.
Dobrze rozpuszcza się w wodzie i metanolu. Dobra substancja redukująca, czasem może jednak być utleniaczem. Słabo zasadowa, tworzy sole, z których najważniejsze to chlorowodorek hydroksyloaminy i siarczan hydroksyloaminy. Sole te są trwalsze niż wolna hydroksyloamina, ale również trujące.
Otrzymywana przez redukcję kwasu azotowego lub tlenków azotu (z wyjątkiem N
2O) w roztworze kwaśnym albo przez działanie zasadą na chlorowodorek lub siarczan hydroksyloaminy i oddestylowanie zmniejszonym ciśnieniem wydzielającej się hydroksyloaminy.
Stosowana jako środek redukujący i odczynnik w syntezie organicznej, np. do otrzymywania oksymów[6]:
- R
2C=O + NH
2OH → R
2C=NOH + H
2O
Działanie hydroksyloaminy na organizm człowieka jest bardzo negatywne. Ma właściwości mutagenne. Reaguje z cytozyną w DNA, zamieniając ją na związek zbliżony do uracylu, działa też na enzymy komórkowe. W wyniku jej działania powstają często groźne mutacje punktowe[7][niewiarygodne źródło?].
Przypisy
- ↑ a b c Neil G. Connelly i inni, Nomenclature of Inorganic Chemistry. IUPAC Recommendations 2005 (Red Book), International Union of Pure and Applied Chemistry, RSC Publishing, 2005, s. 309, ISBN 978-0-85404-438-2 (ang.).
- ↑ a b c d e f g h CRC Handbook of Chemistry and Physics, William M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, s. 4-65, 5-87, 9-63, ISBN 978-1-4987-5429-3 (ang.).
- ↑ a b hydroksyloamina ...% (ang.) w wykazie klasyfikacji i oznakowania Europejskiej Agencji Chemikaliów. [dostęp 2017-01-04].
- ↑ Hydroksyloamina, roztwór (nr 467804) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Polski. [dostęp 2017-01-04]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Hydroksyloamina (nr 467804) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Stanów Zjednoczonych. [dostęp 2017-01-04]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 732. ISBN 83-01-04166-8.
- ↑ Tablice biologiczne, Witold Mizerski (red.) i inni, Warszawa: Adamantan, 2013, s. 302, ISBN 978-83-7350-243-7, OCLC 891265110.
Bibliografia
Media użyte na tej stronie
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
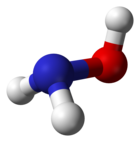
Ball-and-stick model of the hydroxylamine molecule, H2NOH. Bond lengths and angles from CRC Handbook, 88th edition.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for explosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Structural formula of the hydroxylamine molecule, H2NOH. Bond lengths and angles from CRC Handbook, 88th edition.









