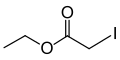
Jodooctan etylu
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | C4H7IO2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory | ICH2COOC2H5 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa | 214,00 g/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | oleista ciecz[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 623-48-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 12183 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | chlorooctan etylu, bromooctan etylu, fluorooctan etylu, jodooctan metylu, octan etylu | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||||
Jodooctan etylu (SK, KSK[a]) – organiczny związek chemiczny, ester etylowy kwasu jodooctowego. Był jednym z najsilniejszych bojowych środków trujących z grupy lakrymatorów stosowanych w czasie I wojny światowej[6].
Otrzymywanie
Jodooctan etylu można otrzymać po dodaniu stałego jodku potasu do alkoholowego roztworu bromooctanu etylu[7][8]. Otrzymanie jodooctanu etylu w sposób analogiczny do chlorooctanu i bromooctanu etylu – poprzez estryfikację kwasu jodooctowego etanolem uważane było dawniej za niemożliwe[7], jednak obecnie synteza taka jest opisana (reakcja w benzenie w obecności stężonego kwasu siarkowego)[9], podobnie jak estryfikacje kwasu jodooctowego innymi alkoholami[10].
Właściwości
Jest to bezbarwna, oleista ciecz o małej lotności. Rozkłada się pod wpływem światła i powietrza, jak również przy długim przechowywaniu, zmieniając barwę na brązową w wyniku uwalniania jodu[3][6]. Bardzo wolno rozkłada się pod wpływem wody i roztworów zasadowych (nieco szybciej przy jednoczesnym ogrzewaniu)[7]:
Jodooctan etylu łatwo reaguje z tiosiarczanem sodu. Jest także całkowicie rozkładany przez ogrzewanie z kwasem azotowym[7].
W celu zwiększenia lotności jodooctanu etylu stosowano go jako mieszaninę z etanolem i octanem etylu. Mieszanina ta, oznaczana skrótem KSK[a], zawierała 70% jodooctanu etylu i 30% etanolu z octanem etylu[3][11]. Stosowana była także mieszanina z chloropikryną (90% jodooctanu etylu i 10% chloropikryny)[3][6].
Zagrożenia
Jodooctan etylu jest lakrymatorem działającym łzawiąco od stężenia 1,4 mg/m³ i toksycznie – 1,5 g/m³ przy 10-minutowej ekspozycji. W kontakcie z oczami powoduje silny ból. Ogólna toksyczność jest ok. 3 razy mniejsza od fosgenu. Z powodu małej lotności, działanie silnie toksyczne jest mało prawdopodobne przy zastosowaniu w otwartym terenie[6].
Jodooctan etylu jest silnym inhibitorem dwóch enzymów z klasy oksydoreduktaz zawierających grupy tiolowe – dehydrogenazy bursztynianowej (EC 1.3.99.1) i oksydazy pirogronianowej (EC 1.2.3.3). Natomiast dehydrogenaza mleczanowa (EC 1.1.1.27) jest całkowicie niewrażliwa na tę substancję[12].
LCt50 wynosi 15 000 mg·min/m³ (860 ppm przy 2-minutowym narażeniu)[3]. W przeglądzie z 1934 roku odnotowano dwa przypadki śmiertelne związane z narażeniem na jodooctan etylu. W pierwszym z nich ofiarą był robotnik wystawiony na działanie tej substancji po wybuchu pocisku, a w drugim – moździerzysta po przedwczesnym wybuchu pocisku[13].
Historia
Po raz pierwszy otrzymany został przez Williama Henry’ego Perkina i Baldwina Francisa Duppę w 1859 roku w reakcji bromooctanu etylu z jodkiem potasu[7][14]. Na początku I wojny światowej jodooctan etylu testowany był przez Brytyjczyków, a w styczniu 1915 roku chemicy z Imperial College London (mieszczącego się w londyńskiej dzielnicy South Kensington – stąd oznaczenie SK[6]) zademonstrowali działanie tego środka bezpośrednio na przedstawicielu Ministerstwa Wojny[15][16].
Został po raz pierwszy użyty 24 września 1915 roku przez Brytyjczyków w bitwie pod Loos[16]. Mimo wyższej ceny jodu w porównaniu do bromu i chloru, był on wykorzystywany do produkcji broni chemicznej z powodu malejących dostaw bromu, podczas gdy jod sprowadzany był w dużych ilościach z Afryki południowej. Roztwory jodooctanu etylu (także w mieszaninie z chloropikryną) m.in. w alkoholu i octanie etylu stosowane były w pociskach haubicznych kal. 4,2″ i w pociskach do moździerzy Stokesa kal. 4″[17]. W 1926 roku wznowiono produkcję jodooctanu etylu w Imperial Chemical Industries[18].
Uwagi
Przypisy
- ↑ a b c d David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 3-246, ISBN 978-1-4200-9084-0 (ang.).
- ↑ a b c d e Jodooctan etylu (nr 242934) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Polski. [dostęp 2011-04-22]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c d e f g Irritating and Lachrymatory Agents C13-A, [w:] D. Hank Ellison, Handbook of Chemical and Biological Warfare Agents, wyd. 2, Boca Raton: CRC Press, 2008, s. 417–418, ISBN 978-0-8493-1434-6 (ang.).Związek C13-A012.
- ↑ a b c Ethyl iodoacetate, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2011-04-22] (ang.).
- ↑ Jodooctan etylu (nr 242934) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Stanów Zjednoczonych. [dostęp 2011-04-22]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b c d e Chemical Warfare Agents. Toxicology and Treatment, Timothy C. Marrs (red.), Robert L. Maynard (red.), Frederick R. Sidell (red.), wyd. 2, John Wiley & Sons, 2007, s. 682, ISBN 978-0-470-01359-5 (ang.).
- ↑ a b c d e Halogenated Esters of Organic Acids. W: Mario Sartori: The War Gases. Chemistry and Analysis. Nowy Jork: Van Nostrand, 1939, s. 121–122. OCLC 2363679.
- ↑ Sidney A. Katz, Harry Salem: Synthesis and Chemical Analysis of Riot Control Agents. W: Riot Control Agents. Issues in toxicology, safety, and health. Eugene J. Olajos, Woodhall Stopford (red.). Boca Raton: CRC Press, 2004, s. 32. ISBN 0-415-29902-0.
- ↑ Catherine Maury, Jean Petrissans. Analyse structurale des dérivés fonctionnels des acides carboxyliques Partie III. Acétate d’éthyle, dérivés α-halogénés. „J. Mol. Struct.”. 249 (2–4), s. 221–232, 1991. DOI: 10.1016/0022-2860(91)85069-F (fr.).
- ↑ Wynik wyszukiwania reakcji CIH2COOH + ROH w bazie reaxys.
- ↑ Chemical Warfare Agents. Toxicology and Treatment, Timothy C. Marrs (red.), Robert L. Maynard (red.), Frederick R. Sidell (red.), wyd. 2, John Wiley & Sons, 2007, s. 688, ISBN 978-0-470-01359-5 (ang.).
- ↑ Corey J. Hilmas i inni, Riot Control Agents, [w:] Handbook of Toxicology of Chemical Warfare Agents, Ramesh C. Gupta (red.), wyd. 1, Elsevier, 2009, s. 159, ISBN 978-0-12-374484-5.
- ↑ Kirby E. Jackson, Margaret Arthur Jackson, Lachrymators, „Chemical Reviews”, 16 (2), 1935, s. 195–242, DOI: 10.1021/cr60054a003 (ang.).c?
- ↑ W. H. Perkin, B. F. Duppa. Ueber die Jodessigsäure. „Justus Liebigs Annalen der Chemie”. 112 (1), s. 125–127, 1859. DOI: 10.1002/jlac.18591120114.
- ↑ Początki – gazy łzawiące i drażniące dymy, [w:] Leszek Konopski, Historia broni chemicznej, Warszawa: Bellona, 2009, s. 30, ISBN 978-83-11-11643-6.
- ↑ a b Corey J. Hilmas, Jeffery K. Smart, Benjamin A. Hill, History of Chemical Warfare, [w:] Medical Aspects of Chemical Warfare, Shirley D. Tuorinsky (red.), Falls Church–Washington: Office of the Surgeon General, U.S. Army–Borden Institute, Walter Reed Army Medical Center, 2008, s. 13, 38, ISBN 978-0-16-081532-4, OCLC 460938576 [zarchiwizowane z adresu 2016-12-01] (ang.).
- ↑ Eric Croddy, Clarisa Perez-Armendariz, John Hart: Chemical and Biological Warfare: A Comprehensive Survey for the Concerned Citizen. Nowy Jork: Springer, 2002, s. 120. ISBN 978-0-387-95076-1.
- ↑ Dwudziestolecie międzywojenne (1918–1939), [w:] Leszek Konopski, Historia broni chemicznej, Warszawa: Bellona, 2009, s. 64, ISBN 978-83-11-11643-6.
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Media użyte na tej stronie
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
The Star of Life, medical symbol used on some ambulances.
Star of Life was designed/created by a National Highway Traffic Safety Administration (US Gov) employee and is thus in the public domain.Skeletal formula of the ethyl iodoacetate molecule, the ester of ethanol and iodoacetic acid.