Korekcja anatomiczna metodą Jatene’a
| ||
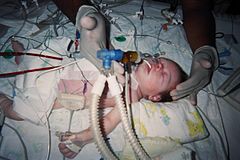 8-dniowy noworodek po operacji Jatene | ||
| ICD-10 | Q20.3 | |
|---|---|---|
Korekcja anatomiczna metodą Jatene’a (ang. Arterial switch operation (ASO) lub Arterial switch) – zabieg kardiochirurgiczny, który jest procedurą na otwartym sercu z użyciem sztucznego płucoserca stosowaną do korygowania przełożenia wielkich naczyń. Przed opracowaniem tej metody, próbowano zastosować dwie inne procedury korekcji na poziomie przedsionków serca, tzw. metodę Senninga i metodę Mustarda[1]. Nazwę tego zabiegu operacyjnego nadano dla uczczenia jego współtwórcy, brazylijskiego kardiochirurga pochodzenia libańskiego Adiba Jatene’a.
Historia opracowania metody
Szkocki anatomopatolog Matthew Baillie w 1797 jako pierwszy opisał przełożenie wielkich pni tętniczych[2]. Przed erą leczenia operacyjnego śmiertelność w pierwszym tygodniu życia wynosiła 30%, do końca pierwszego roku życia dochodziła do 90%[3]. Chorzy, którzy przeżyli, mieli dodatkowe przecieki na poziomie serca lub dużych naczyń (ASD, VSD, PDA) i mieli małą szansę na dożycie wieku dorosłego[4].
W latach 40. XX w. Vivien Thomas (technik chirurgiczny ze szpitala w Baltimore, USA) opracował technikę wytwarzania komunikacji międzyprzedsionkowej bez użycia aparatury do krążenia pozaustrojowego. Z jego doświadczeń skorzystali C. Rollins Hanlon i Alfred Blalock, opracowując metodę procedury paliatywnej zwiększającej mieszanie się krwi na poziomie przedsionków (operacja Blalock-Hanlon)[5]. Ta paliatywna metoda ograniczyła wczesną śmiertelność, ale nie zmniejszyła wskaźników późnej śmiertelności. Po 1966 spadło znaczenie tej metody przez wprowadzenie zabiegu balonowej septektomii metodą Rashkinda tak samo skutecznej, ale stanowiącej mniejsze ryzyko dla pacjenta[6].
Na początku lat 50. William Mustard usiłował przeprowadzić korekcję anatomiczną przełożenia wielkich pni tętniczych. Kilkakrotne próby zakończyły się niepowodzeniem z powodu trudności z przeszczepem naczyń wieńcowych i metoda ta została na dziesięciolecia zarzucona[7].
W 1957 Åke Senning zastosował metodę leczenia przełożenia wielkich pni tętniczych przez korekcję napływu krwi na poziomie przedsionków z użyciem własnych tkanek serca, która znacząco obniżyła śmiertelność wczesną i późną[8].
Ze względu na techniczną złożoność procedury Senninga inni chirurdzy nie uzyskiwali dobrych wyników. W odpowiedzi w 1964 Mustard opisał i wprowadził metodę przekierowania krwi na poziomie przedsionków z użyciem łaty z osierdzia chorego lub z tworzywa sztucznego[9]. Wyniki były porównywalne z metodą Senninga, ale ostatecznie zauważono częste powikłania odległe związane z brakiem wzrostu użytej łaty[10].
W 1975 Adib Jatene przeprowadził pierwszą udaną korekcję anatomiczną u 42-dniowego niemowlęcia z d-TGA i VSD[11]. W 1977 brytyjski kardiochirurg egipskiego pochodzenia Magdi Yacoub umożliwił operowanie dzieci tą metodą w późniejszym okresie życia, wprowadzając zabieg dwuetapowy[12], który następnie został usprawniony[13].
Opis operacji
Po otworzeniu klatki piersiowej przez sternotomię pośrodkową wypreparowuje się aortę do odejścia gałęzi dogłowowych i pień płucny wraz z jej gałęziami do wnęk płucnych celem zwiększenia ich mobilności[14].
Następnie po skaniulowaniu aorty i prawego przedsionka serca przechodzi się na krążenie pozaustrojowe, podczas którego schładza się chorego do 20 °C temperatury rektalnej, co umożliwi późniejsze zatrzymanie krążenia. W celu drenowania lewego serca wprowadza się cewnik do lewego przedsionka przez prawą górną żyłę płucną. Równolegle wypreparowany przetrwały przewód tętniczy po podwójnym podwiązaniu z podkłuciem jest przecinany między podwiązkami. Po schłodzeniu chorego zakleszcza się aortę dosercowo od kaniuli tętniczej i podaje kardiopleginę. Współistniejące ASD lub VSD mogą być aktualnie zamknięte[14].
Po zatrzymaniu krążenia aorta i pień tętnicy płucnej są przecinane tuż powyżej spoideł ich zastawek. Następuje kontrola anatomii naczyń wieńcowych i wycięcie ich ujść z marginesem otaczającej tkanki aortalnej oraz oddzielenie ich proksymalnych odcinków od ściany serca. Po wykonaniu tzw. manewru LeCompte’a, który przywraca przednie położenie pnia płucnego w stosunku do tylnego położenia aorty, dokonuje się reimplantacji ujść tętnic wieńcowych do tzw. neo-aorty (dawna opuszka pnia płucnego) i zespolenia aorty z neo-aortą. Następnie po odpowietrzeniu serca i aorty ponownie włącza się krążenie pozaustrojowe i ogrzewa chorego. Równolegle wykonuje się zespolenie pnia płucnego z byłą opuszką aortalną z użyciem łaty z osierdzia chorego, lub bez. Następnie przeprowadza się kontrolę ewentualnego krwawienia, serce zaopatrywane jest w tymczasowe elektrody nasierdziowe, zakładane są dreny do worka osierdziowego i jam opłucnych[14].
Po ogrzaniu pacjenta, jeżeli stan krążeniowo-oddechowy jest zadowalający, odłącza się sztuczne płucoserce, zamyka klatkę piersiową i przenosi chorego na oddział intensywnej terapii.
Wyniki
W czasie odległych obserwacji zauważono częste występowanie nadzastawkowego zwężenia tętnicy płucnej, które występuje znacznie rzadziej w przypadku bezpośredniego połączenia tętnicy płucnej z byłą opuszką aorty bez użycia łaty z osierdzia[15][16]. Dodatkowo obserwowano postępujące rozszerzenie neoaorty (zastawka płucna po urodzeniu). Jednak rozszerzenie to niekoniecznie przekłada się na niedomykalność aorty (AR) i konieczność operacji u wszystkich pacjentów. Starszy wiek w czasie ASO, obecność ubytku przegrody międzykomorowej są czynnikami ryzyka[17][18].
Przypisy
- ↑ https://books.google.de/books?id=35zSLWyEWbcC&pg=PA515&dq=Arterial+switch+operation&redir_esc=y#v=onepage&q=Arterial%20switch%20operation&f=false | Eric J. Topol; Robert M. Califf; Eric N. Prystowsky; James D. Thomas; Paul D. Thompson. Textbook of Cardiovascular Medicine, s. 515, 2006, ISBN 0-7817-7012-2, data dostępu 2020-11-23, język ang.
- ↑ Baillie M. 2nd ed. London: Johnson and Nicol; 1797. The morbid anatomy of some of the more important parts of the human body; p. 38.
- ↑ John P. Breinholt, Sheba John, Management of the Adult with Arterial Switch, „Methodist DeBakey Cardiovascular Journal”, 15 (2), 2019, s. 133–137, DOI: 10.14797/mdcj-15-2-133, ISSN 1947-6108, PMID: 31384376, PMCID: PMC6668747 [dostęp 2021-01-04].
- ↑ Allen HD, Driscoll DJ, Shaddy RE, Feltes TF. Moss & Adams’ Heart Disease in Infants, Children, and Adolescents: Including the Fetus and Young Adult. 7th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2008. s. 1039–1084.
- ↑ Blalock A, Hanlon CR. The surgical treatment of complete transposition of the aorta and the pulmonary artery. Surg Gynecol Obstet. 1950;90: 1–15.
- ↑ W.J. Rashkind, W.W. Miller, Creation of an atrial septal defect without thoracotomy. A palliative approach to complete transposition of the great arteries, „Journal of the American Medical Association”, 196 (11), 1966, s. 991–992, ISSN 0098-7484, PMID: 4160716 [dostęp 2021-01-04].c?
- ↑ W.T. Mustard i inni, A surgical approach to transposition of the great vessels with extracorporeal circuit, „Surgery”, 36 (1), 1954, s. 31–51, ISSN 0039-6060, PMID: 13178944 [dostęp 2021-01-04].
- ↑ A. Senning, Surgical correction of transposition of the great vessels, „Surgery”, 45 (6), 1959, s. 966–980, ISSN 0039-6060, PMID: 13659340 [dostęp 2021-01-04].
- ↑ W.T. Mustard i inni, THE SURGICAL MANAGEMENT OF TRANSPOSITION OF THE GREAT VESSELS, „The Journal of Thoracic and Cardiovascular Surgery”, 48, 1964, s. 953–958, ISSN 0022-5223, PMID: 14239984 [dostęp 2021-01-04].
- ↑ J.M. Quaegebeur, J. Rohmer, A.G. Brom, Revival of the Senning operation in the treatment of transposition of the great arteries. Preliminary report on recent experience, „Thorax”, 32 (5), 1977, s. 517–524, DOI: 10.1136/thx.32.5.517, ISSN 0040-6376, PMID: 594929, PMCID: PMC470782 [dostęp 2021-01-04].
- ↑ A.D. Jatene i inni, Anatomic correction of transposition of the great vessels, „The Journal of Thoracic and Cardiovascular Surgery”, 72 (3), 1976, s. 364–370, ISSN 0022-5223, PMID: 957754 [dostęp 2021-01-04].
- ↑ M.H. Yacoub, R. Radley-Smith, R. Maclaurin, Two-stage operation for anatomical correction of transposition of the great arteries with intact interventricular septum, „The Lancet”, 1 (8025), 1977, s. 1275–1278, DOI: 10.1016/s0140-6736(77)91317-4, ISSN 0140-6736, PMID: 68381 [dostęp 2021-01-04].c?
- ↑ R.A. Jonas i inni, Rapid, two-stage arterial switch for transposition of the great arteries and intact ventricular septum beyond the neonatal period, „Circulation”, 80 (3 Pt 1), 1989, I203–208, ISSN 0009-7322, PMID: 2766528 [dostęp 2021-01-04].
- ↑ a b c Jacek J. Moll, Marek Kopala, Maciej Moll: Rozdział 14: Całkowite przełożenie dużych naczyń. W: Janusz Skalski, Zbigniew Religa: Kardiochirurgia dziecięca. Katowice: Wydawnictwo Naukowe Śląsk, s. 217–252. ISBN 83-7164-338-1.
- ↑ Kuroczyński W, Kampmann Ch, Peivandi AA, Hartert M, Knuf M, Heinemann MK, Vahl C-F: Mid-term results of a modified arterial switch operation using the direct reconstruction technique of the pulmonary artery. Cardiology Journal, 2010, Vol. 17, No. 6, s. 574–579 | https://journals.viamedica.pl/cardiology_journal/article/view/21305/16909, data dostępu 2021-01-03, jęz. angielski.
- ↑ Moll JJ, Michalak KW, Młudzik K, Moszura T, Kopala M, Moll M, Moll JA.: Long-term outcome of direct neopulmonary artery reconstruction during the arterial switch procedure. Ann Thorac Surg. 2012 Jan;93(1):177-84 | https://www.annalsthoracicsurgery.org/article/S0003-4975(11)02282-X/fulltext | data dostępu 2021-01-03, jęz. angielski.
- ↑ Marathe SP, Talwar S. Surgery for transposition of great arteries: A historical perspective. Ann Pediatr Cardiol. 2015 May-Aug;8(2):122–8. | https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4453180/ | data dostępu 2021-01-03, jęz. angielski.
- ↑ Schwartz ML, Gauvreau K, del Nido P, Mayer JE, Colan SD. Long-term predictors of aortic root dilation and aortic regurgitation after arterial switch operation. Circulation. 2004;110:II128–32.
Linki zewnętrzne
- https://kardiochirurgiadziecieca.cm-uj.krakow.pl/dla-pacjentow/leczone-wady-serca/przelozenie-wielkich-pni-tetniczych-tga/ | dostęp 2020-12-03, jęz. polski
- https://gazetalekarska.pl/?p=54041 | dostęp 2020-12-03, jęz. polski
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Media użyte na tej stronie
The Star of Life, medical symbol used on some ambulances.
Star of Life was designed/created by a National Highway Traffic Safety Administration (US Gov) employee and is thus in the public domain.Autor:
BruceBlaus. When using this image in external sources it can be cited as:
- Blausen.com staff (2014). "Medical gallery of Blausen Medical 2014". WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.010. ISSN 2002-4436.
Arterial Switch Operation. This image was donated by Blausen Medical. Please visit our website to see more medical illustrations and animations.
Eight-day-old d-TGA + VSD, neonate; immediate post-operative (Jatene procedure). Intubation in left nostril; NG tube in right nostril; internal thermometer in mouth/throat; bandaged median sternotomy on chest; EKG leads on chest; pacemaker on abdomen-side; chest tubes emerging from bottom of sternotomy bandage; IV drip in left hand.
Location: PICU at BC Children's Hospital in Vancouver, BC, Canada.
Subject: Amaryllis Kalilah Adoré Nicholson; 8 days old; d-TGA + VSD; Jatene procedure, immediate post-op.


