Krytyczne stężenie micelizacji
Krytyczne stężenie micelizacji (ang. Critical micelle (micellar) concentration, CMC) - w chemii jest definiowane jako stężenie surfaktantów w roztworze, przy którym ich wolne cząsteczki są w równowadze z formami zagregowanymi. Innymi słowy, jest to najmniejsze stężenie surfaktantu, przy którym obecne są agregaty jego cząsteczek (np. micele, a dalsze dodawanie surfaktantu do roztworu nie zwiększa stężenia wolnych cząsteczek, a owocuje tworzeniem się dalszych form zaagregowanych).
Ponadto jest kilka teoretycznych definicji CMC. Jedna z nich mówi, że CMC to całkowite stężenie surfaktantów pod warunkami:
- jeśli C = CMC, (d3F/dCt3) = 0
- F = a[micelli] + b[monomeru]: funkcja roztworu surfaktanta
- Ct: stężenie całkowite
- a, b: stałe propocjonalne
Ponadto wartość CMC jest zależna od metody pomiarowej, ponieważ stałe a i b są z kolei zależne od właściwości roztworu, takich jak: przewodnictwo elektryczne i właściwości fotochemiczne. Kiedy stopień agregacji surfaktantu jest monodyspersyjny, wartość CMC jest niezależna od metody pomiarowej. Z drugiej strony, gdy stopień agregacji jest polidyspersyjny, wartość CMC jest powiązana zarówno z metodą pomiarową, jak i dyspersji (taka sytuacja jest częściej spotykana).
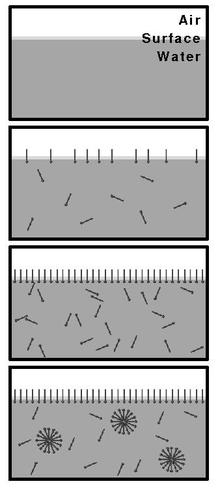
Przykładem polidyspersyjności agregowania są przejścia fazowe zależne od stężenia lipidów. Poniżej CMC lipidy tworzą na powierzchni roztworu monowarstwę, a w roztworze są w postaci monomerycznej (pojedynczych, niezagregowanych cząsteczek). Po przekroczeniu pierwszego CMC (CMC-I), lipidy organizują się w micele, a przy przekroczeniu drugiego CMC (CMC-II) w wydłużone, rurowate struktury micelarne, by powyżej trzeciego CMC (CMC-III), zwanego też punktem lamelarnym, utworzyć stosy, warstwy (lamele) struktur lamelaranych (faza heksagonalna).
Wartości poszczególnych CMC zależne są od budowy związku, jego HLB, co jest wypadkową powierzchni hydrofilowej "głowy" do długości hydrofobowego "ogona".
Bibliografia
- K. S. Birdi: Handbook of surface and colloid chemistry. Boca Raton, Fla.: CRC Press, 1997. ISBN 0-8493-9459-7.
- Paul C. Hiemenz, Raj Rajagopalan: Principles of colloid and surface chemistry. Nowy Jork: Marcel Dekker, 1997. ISBN 0-8247-9397-8.
Media użyte na tej stronie
Autor: Schmin, Licencja: CC BY-SA 3.0
Increasing concentration of surfactant in water eventually forms micelles at or above critical micelle concentration.