Krzemiany
Krzemiany – sole kwasu krzemowego.
Są najliczniejszymi przedstawicielami minerałów:
- ponad 90% skał tworzących skorupę ziemską to krzemiany (60% stanowią skalenie, 12% kwarc, 15% oliwiny, pirokseny i amfibole, a 3% to miki i inne krzemiany).
- prawie 10% stanowi reszta minerałów – przeważnie tlenki (4%), oraz węglany (3%).
Krzemiany są popularnymi minerałami skałotwórczymi.
W przyrodzie występuje około 500 rodzajów krzemianów, z których 40 to minerały bardzo pospolite. Pozostałe spotykane są rzadko. Krzemiany stanowią około 25% wszystkich znanych rodzajów minerałów.
Budowa

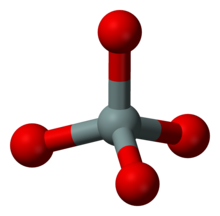
Głównym motywem strukturalnym krzemianów są czworościany (tetraedry) zbudowane z atomu krzemu znajdującego się w środku i otoczonego czterema atomami tlenu umieszczonymi na wierzchołkach.
- We wszystkich krzemianach są stałe grupy krzemotlenowe [SiO4] utworzone przez małe atomy krzemu i duże atomy tlenu. Grupa ta ma silne wiązania, co daje jej dużą stabilność. Owe grupy stanowią zasadniczy składnik budowy krzemianów.
- Drugą cechą charakterystyczną krzemianów jest możliwość zastępowania w ich sieciach krystalicznych atomów krzemu przez atomy glinu. Takie krzemiany noszą nazwę glinokrzemianów. Glin, dzięki swemu promieniowi jonowemu, może zastępować diadochowo krzem w środku czworościanu, a zarazem zachowując się jak kation, łączyć wiązaniami jonowymi tak jak inne metale.
Czworościany utworzone przez grupę [SiO4] mogą łączyć się narożami, mając jeden, dwa, trzy lub cztery wspólne atomy tlenu, zależnie od tego, czy łączą się z jednym, dwoma, trzema czy czterema czworościanami (w taki sposób, że dwie grupy mają wspólny tylko jeden atom tlenu. Powstają w ten sposób łańcuchy, które wiążą kationy metali przez zneutralizowanie ładunków elektrycznych.
Z kolei kationy, w zależności od rozmiarów jonów, mają zdolność wzajemnego zastępowania się, tworząc szeregi izomorficzne.
Złożoność struktur tetraedrycznych zależy głównie od temperatury, w jakiej powstaje minerał. W wysokiej temperaturze tworzą się izolowane czworościany (oliwiny) lub krótkie łańcuchy. W miarę spadku temperatury układ ten komplikuje się, tworząc w końcu trójwymiarowy szkielet (kwarc).
Systematyka krzemianów
| Klasa i typ anionu | Stosunek | Przykład |
|---|---|---|
| Krzemiany wyspowe [SiO4]4- | 4,00:1 | cyrkon Zr[SiO4] |
| Krzemiany grupowe [Si2O7]6- | 3,50:1 | thortveityt Sc2[Si2O7] |
| Krzemiany pierścieniowe [Si3O9]6- [Si4O12]8- [Si6O18]12- [Si8O20]8- [Si12O30]12- | 3,00:1 3,00:1 3,00:1 2,50:1 2,50:1 | pseudowollastonit Ca3Si3O9 baotyt Ba4(Ti,Nb)8[Cl|Si4O12] dioptaz Cu6[Si6O18] • 6H2O ekanit K(Ca,Na)2Th[Si8O20] merriheuetyt (K,Na)2Fe2(Fe,Mg)3[Si12O30] |
| Krzemiany łańcuchowe [Si2O6]4- | 3,00:1 | diopsyd CaMg[Si2O6] |
| Krzemiany wstęgowe [Si4O11]6- | 2,75:1 | tremolit Ca2Mg5[Si8O22](OH)2 |
| Krzemiany warstwowe [Si4O10]4- | 2,50:1 | kaolinit Al4[(OH)8|[Si4O10]] |
| Krzemiany szkieletowe | 2,00:1 | kwarc SiO2 ortoklaz K[AlSi3O8] |
Przykłady krzemianów
- krzemiany wyspowe: willemit, oliwiny, granat, cyrkon, andaluzyt, sylimanit, dysten = kyanit, topaz, staurolit, sfen – tytanit
- krzemiany grupowe: hemimorfit, zoisyt, epidot, wezuwian, prehnit
- krzemiany pierścieniowe: aksynit, beryl, turmalin, dioptaz
- krzemiany łańcuchowe: enstatyt, diopsyd, spodumen, rodonit, wollastonit,
- krzemiany wstęgowe: antofyllit, tremolit, hornblenda
- krzemiany warstwowe: serpentyn, talk, muskowit, biotyt, kaolinit, illit, montmorillonit
- krzemiany szkieletowe: kwarc, opal, skalenie, ortoklaz, plagioklazy, skaleniowce, nefelin, leucyt, lazuryt, zeolity, natrolit, heulandyt.
Zobacz też
Bibliografia
- Podręczny Leksykon Przyrodniczy – Minerały i kamienie szlachetne
- Atlas mineralogii
- Leksykon Przyrodniczy – Minerały
- R. Hochleitner – Minerały i kryształy
- W. Heflik, L. Natkaniec – Nowak – Minerały Polski