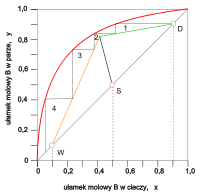
Metoda McCabe’a-Thielego
Metoda McCabe’a i Thielego – prosty graficzny sposób określania liczby półek teoretycznych kolumny rektyfikacyjnej, w której jest rozdzielana mieszanina dwuskładnikowa. Podstawą obliczeń są wyniki badań stanu równowagi ciecz–para oraz wyniki oznaczeń wielkości molowych strumieni destylatu i orosienia oraz stosunku stężeń obu składników w destylowanym roztworze (surowiec, surówka, ciecz surowa), orosieniu i destylacie.
Metoda została opracowana w 1925 przez doktorantów z Massachusetts Institute of Technology (MIT), Warrena L. McCabe’a i Ernesta W. Thielego[1]. Jest stosowana w sytuacjach, gdy:
- molowe ciepła parowania składników surówki można uznać za jednakowe
- na każdy mol odparowującej cieczy kondensuje jeden mol pary
- przenikanie ciepła do i z kolumny destylacyjnej jest znikome
Podstawą metody jest bilans materiałowy procesu.
Przebieg wyznaczania liczby półek teoretycznych
krok po kroku (1)


krok po kroku (2)
Przed rozpoczęciem oznaczenia liczby półek teoretycznych w określonej kolumnie rektyfikacyjnej trzeba uzyskać dane dotyczące równowagi ciecz–para w testowym układzie dwuskładnikowym A + B (B – składnik bardziej lotny). W czasie rektyfikacji roztworu testowego oznacza się wielkości strumieni destylatu i orosienia (liczba moli na godzinę) oraz stężenia składników w destylacie, surówce i cieczy wyczerpanej (ułamki molowe).
Sporządzany jest wykres w układzie współrzędnych:
- oś odciętych – x, ułamek molowy B w cieczy
- oś rzędnych – y, ułamek molowy B w parze
W pierwszej kolejności wykreśla się:
- linię pomocniczą x = y (przekątna kwadratu)
- linię równowagi – zależność ułamka molowego B w parze od ułamka molowego B w cieczy
- linie pionowe, określające ułamek molowy B w surówce, destylacie i cieczy wyczerpanej
W następnej kolejności wykreśla się tzw. górną linię operacyjną, dla tej części kolumny, która znajduje się nad punktem odpowiadającym składowi surówki (większe stężenie składnika bardziej lotnego). W tym celu z punktu przecięcia linii składu destylatu z linią pomocniczą x = y wykreśla się prostą o nachyleniu[2][a]:
- Δy / Δx = R / (D + R)
gdzie:
- D – molowy strumień odbieranego destylatu (np. liczba moli na godzinę)
- R – molowy strumień kondensatu zawracanego do kolumny, zwanego orosieniem.
- D – molowy strumień odbieranego destylatu (np. liczba moli na godzinę)
Przykład:
- orosienie: R = 2000 moli/h
- destylat: D = 1000 moli/h
- nachylenie linii operacyjnej: 2000 / (2000 + 1000) = 2/3 = 0,67
- destylat: D = 1000 moli/h
W kolejnym etapie jest wykreślana tak zwana „linia q”. Parametr q określa termodynamiczny stan surówki. Jest zdefiniowany jako ułamek molowy cieczy w surówce, która może być np. mieszaniną cieczy i pary, parą nasyconą bez cieczy lub cieczą o temperaturze niższej od temperatury wrzenia.
Współczynnik nachylenia „linii q” oblicza się jako:
- Δy / Δx = q / (q - 1).
Przypadki charakterystyczne:
- surowiec jest cieczą o temperaturze wrzenia, nie zawierającą pary:
- q = 1, Δy / Δx = nieskończoność, linia q jest równoległa do osi rzędnych (pionowa)
- surowiec jest parą nasyconą nie zawierającą cieczy:
- q = 0, Δy / Δx = 0 , linia q jest równoległa do osi odciętych (pozioma)
- udziały cieczy i pary w surowcu są jednakowe:
- q = 0,5 Δy / Δx = -1, linia q ma nachylenie 135o
W przypadkach, gdy surowiec jest przegrzaną parą lub ochłodzoną cieczą, z punktu przecięcia linii składu destylatu z linią x = y wykreśla się linie q najmniej odchylone od linii x = y, biegnące w górę (ochłodzona ciecz) lub w dół (nagrzana para).
Po wykreśleniu linii q przeprowadza się linię operacyjną dolną. Jest to prosta łącząca punkty przecięcia prostej x = y z linią q i z linią składu cieczy wyczerpanej.
Ostatnim etapem procedury jest wykreślenie krzywej schodkowej między liniami operacyjnymi i linią równowagi fazowej, rozpoczynając od punktu przecięcia prostej x = y z linią składu destylatu. Liczba uzyskanych stopni określa liczbę półek teoretycznych w badanej kolumnie.
Uwagi
Przypisy
- ↑ Mccabe i Thiele 1925 ↓.
- ↑ Ciborowski 1955 ↓, s. 645.
- ↑ Ciborowski 1965 ↓, s. 511–512.
Bibliografia
- Janusz Ciborowski: Podstawy inżynierii chemicznej. Warszawa: Wydawnictwo Naukowo-Techniczne, 1965, s. 515-530. (pol.).
- Janusz Ciborowski: Inżynieria chemiczna. Wyd. 2. Warszawa: Wydawnictwo Naukowo-Techniczne, 1955, s. 644-680. (pol.).
Linki zewnętrzne
- W. L. Mccabe, E. W. Thiele. Graphical Design of Fractionating Columns. „Ind. Eng. Chem.”, s. 605–611, czerwiec 1925. DOI: 10.1021/ie50186a023. (ang.).
- Tore Haug-Warberg, Norwegian University of Science and Technology, Norway: Detailed discussion of McCabe-Thiele method. [dostęp 2015-02-18]. (ang.).
- Ming T. Tham: More detailed information on how to draw a McCabe-Thiele Diagram. [dostęp 2011-01-06]. (ang.).
- João Fernando Pereira Gomes. Reflections on the use of the McCabe and Thiele method. „Revista Ciências & Tecnologia”. 1 (1), s. 1–7, julho-dezembro 2007. Universidade Católica de Pernambuco.
- McCabe-Thiele Diagram generator. [dostęp 2011-01-06]. (ang.).
Media użyte na tej stronie
Metoda McCabe'a-Thielego - 4
Metoda McCabe'a i Thielego - wykres x-y 3
Metoda McCabe'a i Thielego - 7
Metoda Cabe'a i Thielego - 6
Metoda McCabe'a-Thielego - wykres równowagi x-y
Metoda McCabe'a-Thielego - wykres T-x
Metoda McCabe'a i Thielego - 8
Metoda McCabe'a i Thielego - 5
Metoda McCabe'a-Thielego 1
Palec chłodzący (prosty deflegmator laboratoryjny)