Ośmiornice
| Octopoda[1] | |||
| Leach, 1818 | |||
| Okres istnienia: pensylwan-obecnie 323,2–0 mln lat temu | |||
 Octopus macropus | |||
| Systematyka | |||
| Domena | |||
|---|---|---|---|
| Królestwo | |||
| Typ | |||
| Podtyp | |||
| Gromada | |||
| Podgromada | |||
| Rząd | ośmiornice | ||
| Podrzędy | |||
| |||
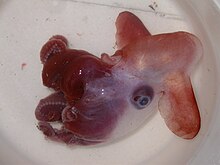
Ośmiornice (Octopoda) – rząd głowonogów, ośmioramiennych mięczaków, do którego zaliczono około 300 gatunków. Są to zwierzęta dwubocznie symetryczne, mają dwoje oczu i dziób oraz otwór gębowy usytuowany w centralnym punkcie względem ramion. Ich gibkie ciało odznacza się ogromnymi możliwościami, jeśli chodzi o zakres ruchu. Do przemieszczania się odrzutem zwierzę wykorzystuje syfon, przez który wyrzuca wodę; głowa podczas pływania znajduje się na przodzie, wzniesiona. Syfon służy także wymianie gazowej. Ośmiornice mają złożony układ nerwowy, a większość gatunków odznacza się świetnym wzrokiem. Należą też do najinteligentniejszych bezkręgowców, prezentujących najbardziej złożone zachowania.
Zamieszkują zróżnicowane regiony oceanów, w tym rafy koralowe, wody pelagiczne i dno morskie (zob. bentos, bental). Niektóre żyją w strefie międzypływowej, inne zasiedlają abisal. Większość gatunków charakteryzuje się szybkim wzrostem osobniczym, wczesnym dojrzewaniem i krótkim życiem. W okresie rozrodczym samiec zapładnia samicę, po czym starzeje się i umiera. Samica składa zapłodnione jaja w norze i opiekuje się nimi aż do wylęgu młodych, po czym również ginie.
Strategie obrony przed drapieżnikami obejmują: wyrzucenie sepii, kamuflaż i odstraszanie, wykorzystanie ruchu odrzutowego i ukrywanie się. Wszystkie ośmiornice dysponują jadem, ale tylko Hapalochlaena może doprowadzić do śmierci człowieka.
Etymologia
Łacińska nazwa naukowa ośmiornicy octopus ma swój źródłosłów w starożytnej grece. Pochodzi od słowa ὀκτώπους, ὀκτά-, które jest złożeniem formy ὀκτώ (oktō, 8) z wyrazem πούς (pous, stopa). Używał jej na przykład Aleksander z Tralles (ok. 525 – ok. 605)[2][3][4].
Anatomia i fizjologia
Wielkość

Za największy znany gatunek ośmiornic uważa się ośmiornicę olbrzymią, której osobniki dorosłe osiągają masę 15 kg i rozpiętość ramion 4,3 m[5]. Największy udokumentowany naukowo osobnik tego gatunku ważył 71 kg[6]. Donoszono też o osobnikach znacznie większych[7]: jeden ważył 272 kg z rozpiętością ramion 9 m[8]. Znaleziono ciało nieżywego osobnika Haliphron atlanticus ważące 61 kg, którego masę życiową oceniono na 75 kg[9][10].
Najmniejszy gatunek to Octopus wolfi, dorastający do około 2,5 cm i ważący poniżej 1 g[11].
Morfologia
Ośmiornice wykazują symetrię dwuboczną o osi grzbietowo-brzusznej. Przedni koniec wydłużonego ciała stanowią głowa i stopa. Na głowie znajdują się oczy i syfon. Stopa wyewoluowała w grupę giętkich, chwytnych ramion, które otaczają otwór gębowy, a u podstawy łączą się z sobą błoną międzyramieniową[12]. Ramiona można podzielić na cztery pary; opisuje się je, biorąc pod uwagę stronę i kolejność (np. L1, R1, L2, R2)[13][12]. Dwa ostatnie ramiona na ogół służą zwierzęciu do przemieszczania się po dnie morskim, pozostałe sześć zaś – do poszukiwania pożywienia. Z tego powodu niektórzy naukowcy uważają, że ośmiornice mają sześć „rąk” i dwie „nogi”[14][15]. Tylną część ciała stanowi dobrze umięśniony płaszcz w kształcie pustego w środku, owalnego worka. Zawiera on większość niezbędnych do życia narządów, w tym skrzela[16][17]. Jama płaszczowa, ograniczona ścianami mięśniowymi, łączy się ze środowiskiem zewnętrznym za pomocą lejka, czyli syfonu[12][18]. Pod ramionami znajduje się otwór gębowy zaopatrzony w ostry, twardy dziób[17].
Skórę tworzą gruby naskórek z komórkami śluzowymi i czuciowymi oraz zbudowana z tkanki łącznej skóra właściwa, składająca się głównie z włókien kolagenu i komórek zawierającej chromatofory, umożliwiających zmianę barwy[12]. Większą część ciała buduje tkanka miękka pozwalająca na wydłużanie, kurczenie i zwijanie ramion, głowy i płaszcza. Dzięki temu ośmiornica może się przeciskać przez wąskie szczeliny. Nawet przedstawiciele większych gatunków potrafią się przedostać przez otwór mierzący jedynie 2,5 cm średnicy[17]. Ramiona nie opierają się na żadnym szkielecie, lecz pracują na zasadzie hydrostatyki. Zawierają mięśnie podłużne, poprzeczne i okrężne, ułożone wokół biegnącego przez środek ramienia nerwu osiowego. Ramiona mają ogromne możliwości ruchowe: mogą się wydłużać i skracać, skręcać w lewo i prawo, zginać w dowolnym miejscu i kierunku bądź też trzymać się sztywno[19][20] – na takiej samej zasadzie opiera się działanie języka u ssaków[21].
Wewnętrzna powierzchnia każdego z ramion pokryta jest ułożonymi w dwa rzędy okrągłymi, miseczkowatymi przyssawkami, które pozwalają zwierzęciu przylgnąć mocno do czegoś bądź manipulować przedmiotami. W każdej przyssawce wyróżnia się dwie odrębne części: zewnętrzną płytką jamkę zwaną infundibulum oraz środkową, pustą przestrzeń nazywaną acetabulum; obie pokrywa gruba warstwa mięśni w kutykulowej osłonce. Kiedy przyssawka przylega do jakiejś powierzchni, uszczelnia się rozdzielający je otwór. Infundibulum zapewnia adhezję, podczas gdy odłączone od niego acetabulum przy odpowiednich skurczach mięśni pozwala albo na przylgnięcie, albo na odłączenie się[22][23].
Oczy ośmiornic są duże, usytuowane w górnej części głowy i osadzone w chrzęstnej osłonce, połączonej z puszką chrzęstną mózgu. Budową przypominają oczy rybie. Rogówkę tworzy półprzezroczysta warstwa naskórka. Położona za nią szczelinowata źrenica to otwór w tęczówce. Za źrenicą znajduje się soczewka. Tył wnętrza gałki ocznej jest wyścielony światłoczułymi komórkami siatkówki. Źrenica może dostosowywać swą wielkość do ilości światła, a pigment siatkówki pochłania padające światło o dużej jasności[12]. Dobrze rozwinięte oczy widzą światło spolaryzowane, co najprawdopodobniej przekłada się na zdolność dobrego widzenia[24][25].
Niektóre gatunki mają inny od typowego dla ośmiornic kształt ciała. Przedstawiciele podrzędu frędzlikowców odznaczają się korpulentnym, galaretowatym ciałem z błoną międzyramienną sięgającą szczytów ramion oraz dwiema dużymi płetwami powyżej oczu, wspartymi na muszli wewnętrznej. Dolną część ramion u tych ośmiornic pokrywają mięsiste brodawki zwane cirri.
Układ krążenia
Ośmiornice mają zamknięty układ krążenia – krew pozostaje w obrębie naczyń krwionośnych – oraz trzy serca: jedno układowe, pompujące krew przez ciało, i dwa serca skrzelowe, które przepompowują ją przez skrzela. Serce układowe nie działa, kiedy zwierzę pływa, dlatego też ośmiornica, płynąc, szybko się męczy i preferuje pełzanie[26][27].
Krew zawiera bogate w miedź białko hemocyjaninę, transportującą tlen. Zwiększa ona lepkość krwi, co sprawia, że przepompowanie krwi przez ciało wymaga znacznego ciśnienia. Ciśnienie tętnicze może więc przekraczać 75 mmHg[26][27][28]. W chłodnych warunkach o niskiej dostępności tlenu hemocyjanina transportuje go wydajniej od hemoglobiny. Hemocyjanina – przeciwnie do hemoglobiny, która znajduje się w czerwonych krwinkach – jest rozpuszczona w osoczu i nadaje krwi niebieskawy kolor[26][27].
Serce układowe składa się z trzech jam o mięśniowych ścianach: jednej komory i dwóch przedsionków. Naczynia krwionośne – tętnice, naczynia włosowate i żyły – są wyścielone nabłonkiem nietypowym dla bezkręgowców. Krew wypływa z serca układowego przez aortę i tętnice do naczyń włosowatych, po czym do żył i wreszcie do żyły głównej (czczej), po czym pompowana jest dalej do skrzeli przez serca skrzelowe i wraca do serca układowego. Większość układu żylnego ma zdolność kurczenia się, podobnie jak tętnice, co wspomaga przepływ krwi[12].
Wymiana gazowa
Wymiana gazowa u ośmiornic polega na wciągnięciu wody do jamy płaszczowej przez otwór, przepuszczeniu jej przez skrzela i pozbyciu się przez syfon. Woda wpływa do jamy płaszczowej dzięki skurczowi promienistych mięśni ściany płaszcza, po czym silne mięśnie okrężne wyrzucają wodę przez syfon, czemu towarzyszy zamknięcie zastawek. Mięśnie oddechowe wspiera rozległa sieć tkanki łącznej, umożliwiająca im rozszerzanie komory oddechowej[29]. Blaszkowata budowa skrzeli pozwala na znaczny pobór tlenu, aż do 65% w wodzie o temperaturze 20⁰C[30]. Przepływ wody przez skrzela jest skorelowany z poruszaniem się zwierzęcia. Ośmiornica może przemieścić się siłą odrzutu, wypychając wodę przez syfon[29][28].
Tlen jest także wchłaniany przez cienką skórę ośmiornic. Oszacowano, że w trakcie spoczynku zwierzę może w ten sposób pokrywać do 41% zapotrzebowania na tlen. Podczas pływania ośmiornice wprawdzie wchłaniają przez skórę jeszcze większą ilość tlenu, jednak udział ten maleje wówczas do 33%, gdyż znacznie więcej wody przepływa przez skrzela. Dlatego bezwzględna intensywność jego wchłaniania tą drogą rośnie bardziej niż w przypadku drogi przez skórę. Z drugiej strony u ośmiornicy zwiniętej w jamie, trawiącej pokarm po sutym posiłku, udział ten może obniżyć się do 3% całkowitego zapotrzebowania na tlen[31].
Trawienie i wydalanie
Układ pokarmowy ośmiornicy zaczyna się masą gębową (masą bukalną) składającą się z jamy gębowej, gardła, tarki (raduli) i gruczołów ślinowych[32]. Zanim zdobycz trafi do jamy gębowej, jest rozszarpywana twardymi, mocnymi szczękami w kształcie dzioba. Następnie pokarm zostaje rozdrobniony przez tarkę – pokryty zadziorkami, przypominający język narząd zbudowany z chityny[17]. Dalej tarka i dwa boczne wyrostki ścian przełyku przepychają porcję pokarmu do przełyku. Kolejno pokarm przechodzi do przewodu żołądkowo-jelitowego, w większej części podwieszonego u góry jamy płaszczowej za pomocą licznych błon. Przewód składa się z wola, przechowującego pokarm; z żołądka, w którym pokarm jest trawiony; z caecum, czyli kieszeni żołądka, gdzie nadtrawiona papka pokarmowa rozdziela się na frakcję płynną i stałą, co jest niezwykle ważne dla wchłaniania; z wątrobotrzustki, której hepatocyty rozkładają i wchłaniają płyny; oraz z jelita, gdzie zbierają się odpady i tworzą się z nich sznury kałowe, wyrzucane ostatecznie przez odbyt[32][33].
W ramach osmoregulacji płyn z serc skrzelowych dostaje się do osierdzia. Ośmiornica ma dwa nefrydia (odpowiedniki nerek kręgowców) związane z sercami skrzelowymi. Nefrydia i ich przewody łączą jamę płaszczową z jamami osierdziowymi. Przed dotarciem do serca skrzelowego każde odgałęzienie żyły czczej poszerza się, tworząc wyrostki nerkowe pozostające w bezpośrednim kontakcie z cienkościennym nefrydium. Mocz najpierw powstaje w jamie osierdzia, a potem, kiedy przepływa przez przewód i nefrydiopor do jamy płaszczowej, jest modyfikowany: w wyrostkach nerkowych odbywa się selektywna absorpcja, a wydalony zostaje głównie amoniak[12][34].
Układ nerwowy i zmysły
Ośmiornice (oraz mątwy) cechuje najwyższy współczynnik masy mózgu do ciała spośród wszystkich bezkręgowców, przekraczający nawet wartości osiągane przez część kręgowców[35]. Na wysoce złożony układ nerwowy w około jednej trzeciej składa się mózg zamknięty w puszce chrzęstnej[36]. Dwie trzecie neuronów ośmiornicy znajduje się w nerwach ramion, wykazujących wachlarz złożonych odruchów działających także bez połączenia z mózgiem[37]. W przeciwieństwie do kręgowców złożone zdolności motoryczne ośmiornic nie są organizowane w mózgu przez wewnętrzną mapę ciała – zamiast tego działa niesomatotopowy system występujący tylko u bezkręgowców o dużych mózgach[38].
Większość gatunków ośmiornic ma dobry wzrok. Jak inne głowonogi, rozróżniają polaryzację światła. Widzenie barwne wydaje się różnić między gatunkami. Przykładowo występuje u Octopus aegina, ale nie u O. vulgaris[39]. Istnieją też gatunki prawie ślepe, wśród których wymienia się Cirrothauma murrayi[40].
Obok mózgu znajdują się dwa specjalne narządy zwane statocystami. Są to workowate struktury zawierające kryształki minerałów i włoski czuciowe. Umożliwiają one ośmiornicy orientację przestrzenną. Dostarczają informacji o pozycji ciała względem grawitacji i potrafią wykrywać przyśpieszenie kątowe. Autonomiczny układ nerwowy utrzymuje oczy ośmiornicy w taki sposób, że źrenica zawsze leży poziomo[12]. Statocysty służyć mogą także do słyszenia dźwięków. Ośmiornica zwyczajna słyszy dźwięki między 400 Hz a 1000 Hz, a najlepiej o częstotliwości 600 Hz[41].
Zmysł dotyku również jest świetnie rozwinięty. Przyssawki zawierają chemoreceptory umożliwiające ośmiornicy rozpoznawanie smaku podczas dotykania. Ramiona nie plączą się ani nie zderzają jedne z drugim, ponieważ receptory rozpoznają skórę ośmiornicy i chronią przed sczepianiem się ze sobą[42].
W ramionach są usytuowane receptory napięcia, dzięki którym zwierzę wie, czy jego ramiona są wyciągnięte, nie wystarcza to jednak mózgowi, by określić pozycję ciała bądź ramion. W efekcie ośmiornica nie ma zdolności stereognozji, co oznacza, że nie tworzy reprezentacji ogólnego kształtu przedmiotu, który trzyma. Potrafi wykryć lokalne zmiany tekstury, jednak nie umie zintegrować tych informacji, tworząc większy obraz. Autonomia neurologiczna ramion stwarza wielką trudność w uczeniu szczegółowych skutków ich ruchów. Propriocepcja jest słaba – mięczak wie jedynie, jakie dokładnie ruchy wykonuje, widząc ramiona[43].
Woreczek czernidłowy
Woreczek czernidłowy ośmiornicy mieści się poniżej gruczołu trawiennego. Przyłączony do woreczka gruczoł produkuje sepię, magazynowaną w woreczku. Narząd ten znajduje się na tyle blisko lejka, by ośmiornica mogła wyrzucić zawartość w strumieniu wody. Przed opuszczeniem lejka sepia przechodzi przez gruczoły, mieszając się ze śluzem i tworząc w wodzie gęstą, czarną plamę umożliwiającą mięczakowi ucieczkę przed drapieżnikiem[44]. Głównym pigmentem sepii jest melanina, której zawdzięcza ona barwę czarną[45]. Cirrhina nie mają woreczka czernidłowego[46].
Cykl życiowy
Rozmnażanie
Ośmiornice są rozdzielnopłciowe. Każdy osobnik ma jedną, leżącą w tylnej części ciała gonadę połączoną z jamą ciała. Jądro samca i jajnik samicy wybrzusza się do gonocelu, dokąd uwalniane są gamety. Gonocel łączy się poprzez gonodukt z jamą płaszczową, do której dostaje się przez gonopor[12]. Kulisty gruczoł wzrokowy wytwarza hormony powodujące dojrzewanie i starzenie organizmu oraz stymulujące produkcję gamet. Jego pracę mogą zaburzać czynniki środowiskowe, jak temperatura, światło i dostępność pokarmu, kontrolujące rozród i długość życia[47][48].
Podczas rozrodu samiec wykorzystuje wyspecjalizowane ramię o nazwie hektokotylus, by przenieść spermatofor (pakiet nasienia) z końcowego narządu swego przewodu rozrodczego do jamy płaszczowej samicy[49]. U ośmiornic bentosowych hektokotylusem jest zazwyczaj trzecie ramię po prawej stronie, zaopatrzone w łyżkowate zagłębienie i zmodyfikowane przyssawki w okolicy czubka. U większości gatunków zapłodnienie odbywa się w jamie płaszczowej samicy[12].
Rozmnażanie ośmiornic zbadano tylko w przypadku kilku gatunków. U ośmiornicy olbrzymiej godom towarzyszą zmiany tekstury i barwy skóry. Samiec może uczepić się górnej bądź bocznej części ciała samicy albo zająć pozycję przed nią. Przypuszcza się, że może najpierw za pomocą swego hektokotyla usunąć spermatofor lub spermę już obecną w samicy. Podnosi spermatofor ze swego woreczka hektokotylem, wkłada go do jamy płaszczowej samicy i zostawia w miejscu właściwym dla gatunku. W przypadku ośmiornicy olbrzymiej jest to ujście jajowodu. Tą drogą transportowane są dwa spermatofory, jest to około metra długości, a pusty koniec może wybrzuszać się z płaszcza samicy[50]. Złożony mechanizm hydrauliczny uwalnia nasienie ze spermatoforu, po czym jest ono przechowywane w ciele samicy[12].

Około czterdziestu dni po współżyciu samica ośmiornicy olbrzymiej przymocowuje sznury zapłodnionych jaj (w sumie od 10000 do 70000) do skał w szczelinie bądź pod występem skalnym, gdzie strzeże ich i opiekuje się nimi przez mniej więcej pięć miesięcy (160 dni), nim wyklują się młode[50]. W zimniejszych wodach, na przykład opływających Alaskę, może minąć 10 miesięcy, zanim jaja będą gotowe do wylęgu[51]. Matka napowietrza je i dba o ich czystość. Jeśli zostaną pozostawione same sobie, z wielu z nich nic się nie wykluje[52]. Samica nie spożywa pożywienia w czasie opieki nad jajami i krótko po wylęgu ginie. Samce starzeją się i umierają kilka tygodni po współżyciu[53].
Jaja mają duży zapas żółtka. Bruzdkowanie jest powierzchniowe. Tarczka zarodkowa rozwija się u bieguna. Podczas gastrulacji jej brzegi rosną do dołu i otaczają żółtko, wytwarzając pęcherzyk żółtkowy, z którego w kiedyś powstanie część jelita. Grzbietowa strona tarczki rośnie w górę i tworzy zarodek z gruczołem muszlowym na jego powierzchni grzbietowej, a ponadto ze skrzelami, płaszczem i oczami. Ramiona i lejek rozwijają się jako część stopy z brzusznej strony tarczki. Ramiona później migrują do góry, tworząc pierścień wokół lejka i otworu gębowego. Żółtko jest stopniowo wchłaniane w trakcie rozwoju zarodka[12].

Większość młodych ośmiornic wylęga się z jaj w postaci paralarwy, po czym prowadzi przez tygodnie lub miesiące planktoniczny tryb życia, zależnie od gatunku i temperatury wody. Żywią się one wtedy widłonogami, larwami stawonogów i innym zooplanktonem, aż w końcu opadają na dno oceaniczne i rozwijają się bezpośrednio w dojrzałe osobniki bez wyodrębnionej metamorfozy obserwowanej u innych grup mięczaków[12]. Niektóre gatunki składające większe jaja – należą do nich: Hapalochlaena maculosa, Octopus briareus, Octopus bimaculoides i Eledone moschata[54] – oraz zamieszkujące głębokie morza nie mają etapu paralarwy, z jaja wylęga się u nich bentosowe zwierzę przypominające osobnika dorosłego[51][55].
U żeglarków samica wydziela cienką jak papier, żłobkowaną muszlę, do której składa jaja i w której także przebywa, unosząc się w toni morskiej. Tam też wylęgają się młode, ponadto muszla pomaga jej utrzymać odpowiednią wyporność i schodzić głębiej. Samiec tego rodzaju jest niewielki i nie ma muszli[56].
Długość życia
Ośmiornice mają stosunkowo krótki okres życia. U niektórych gatunków wynosi zaledwie sześć miesięcy. Ośmiornica olbrzymia, jeden z dwóch największych gatunków, może dożyć pięciu lat. Długość życia ośmiornic ogranicza rozmnażanie: samce żyją tylko kilka miesięcy po połączeniu się z samicą, te ostatnie z kolei umierają krótko po wylęgnięciu się młodych z jaj. Narządy rozrodcze dojrzewają dzięki wpływowi hormonów gruczołu wzrokowego, ale w efekcie dochodzi do dezaktywacji gruczołów trawiennych, co zazwyczaj powoduje śmierć głodową[57]. Eksperymentalne usunięcie obu gruczołów wzrokowych po rozrodzie skutkuje przerwaniem opieki nad potomstwem, wznowieniem pobierania pokarmu, zwiększonym wzrostem i znacznie zwiększa długość życia[58].
Rozmieszczenie geograficzne i siedlisko

Ośmiornice żyją w każdym oceanie. Poszczególne gatunki zaadaptowały się do różnych siedlisk morskich. Jako osobniki młodociane ośmiornice zwyczajne zasiedlają płytkie baseny pływowe. Ośmiornica hawajska Octopus cyanea zamieszkuje rafy koralowe. Żeglarek dryfuje w pelagialu. Abdopus aculeatus żyje głównie w przybrzeżnych trawach morskich. Niektóre gatunki przystosowały się do zimnych głębin oceanicznych. Bathypolypus arcticus spotyka się na równinach abisalnych leżących 1000 m pod poziomem morza. Vulcanoctopus hydrothermalis trzyma się w pobliżu kominów hydrotermalnych na głębokości 2000 m[16]. Frędzlikowce często wolno pływają i zamieszkują głębokie wody[59]. Gatunek Grimpoteuthis (ośmiornica dumbo) sfotografowano na głębokości 6957 m (22,825 ft)[60]. Żaden gatunek nie zasiedla jednak wód słodkich[61].
Zachowanie i ekologia
Większość gatunków z wyjątkiem rozrodu wiedzie samotny tryb życia[62], jest jednak kilka znanych nauce gatunków pojawiających się w dużym zagęszczeniu i udzielających częstych interakcji, przesyłania pomiędzy sobą sygnałów, obrony partnera i usuwania innych osobników z jam. Stanowi to prawdopodobnie wynik dużej obfitości pożywienia przy ograniczonej liczbie dostępnych jam[63]. Ośmiornice ukrywają się bowiem w jamach, zazwyczaj w szczelinach skalnych lub w innych twardych strukturach, choć niektóre gatunki potrafią drążyć jamy w piasku czy mule. Nie występuje terytorializm, ale zwierzęta ogólnie pozostają w swych rewirach, które opuszczać mogą w poszukiwaniu pokarmu. Wykorzystują swe umiejętności nawigacyjne, by wrócić do jamy bez cofania się po przebytej uprzednio drodze[64]. Nie wiadomo by migrowały[65].
Ośmiornice zabierają złapaną zdobycz do swej jamy, gdzie mogą ją bezpiecznie skonsumować. Czasami zwierzę chwyta więcej pokarmu niż może spożyć i jamę często otacza sterta odpadów martwych i niedojedzonych posiłków mięczaka. Jamę z ośmiornicą dzielą często inne stworzenia, jak ryby, kraby, inne mięczaki i jeżowce. Niektóre przybyły skuszone padliną, inne przeżyły zawleczenie ich przez ośmiornicę[66].
Pożywienie
Prawie wszystkie ośmiornice są drapieżne. Te zamieszkujące dno morskie zjadają głównie skorupiaki, wieloszczety i inne mięczaki, jak zwójki i małże. Ośmiornice otwartego morza jedzą głównie krewetki, ryby i inne głowonogi[67]. Większość dań w diecie ośmiornicy olbrzymiej to małże takie jak sercówki Clinocardium nuttallii czy przegrzebki i skorupiaki takie jak kraby czy Majoidea. Odrzucają natomiast ślimaki Naticidae z powodu nadmiernych rozmiarów oraz czareczki, Crassadoma, chitony i Haliotis jako zbyt mocno przytwierdzone do podłoża[66].
Ośmiornice zasiedlające dno morskie zazwyczaj przemieszczają się między skałami i przełażą przez szczeliny. Osobnik może zaatakować ofiarę siłą odrzutu i pociągnąć do jamy ustnej swymi ramionami, przytrzymując ją przyssawkami. Małą zdobycz zamyka w całości błona międzyramieniowa. Ośmiornica zwykle traktuje skorupiaki takie jak kraby paraliżującą śliną, po czym kawałkuje je dziobem[67][68]. Ośmiornice zjadają mięczaki chronione muszlą dzięki siłowemu oddzielaniu muszli bądź wywiercaniu dziurki, przez którą podają neurotoksynę[69][68]. Myślano, że otwór taki wierciły tarkami, ale okazało się, że działają tutaj niewielkie ząbki na szczycie gruczołu ślinowego, a enzym obecny w toksycznej ślinie roztwarza węglan wapnia budujący muszlę. Ośmiornica pospolita potrzebuje około trzech godzin, aby wywiercić dziurkę średnicy 0,6 mm. Po spenetrowaniu muszli zdobycz ginie prawie natychmiast, jej mięśnie rozkurczają się, a tkanki miękkie są już łatwe do zdobycia. Kraby również można uśmiercać w ten sposób. Gatunki o grubej muszli z większą szansą będą przewiercane, kraby o muszli cienkiej są rozdzierane[70].
Niektóre gatunki mają inne sposoby żywienia się. Grimpoteuthis cechuje się zredukowaną tarką bądź jej brakiem i połyka zdobycz w całości[46]. U głębokomorskiej Stauroteuthis niektóre miocyty kontrolujące przyssawki u większości gatunków zastąpiły fotofory. Uważa się, że mylą one zdobycz, kierując ją do jamy ustnej drapieżnika, czyniąc go jedną z niewielu bioluminescentnych ośmiornic[71].
Poruszanie się
Ośmiornice przemieszczają się, głównie względnie wolno pełznąc, niekiedy pływając z głową od przodu. Pływanie w tył lub odrzutowe jest ich najszybszym sposobem przemieszczania się, następnie zaś zwykłe pływanie i pełzanie[72]. Kiedy nie trzeba się śpieszyć, zwierzę zwykle pełznie po twardych lub miękkich podłożach. Kilka ramion wysuwa się do przodu, część przyssawek przywiera do podłoża i zwierzę przeciąga się do przodu dzięki silnym mięśniom ramion, podczas gdy inne ramiona raczej pchają niż ciągną. Z posuwaniem się inne ramiona wędrują za głowę, przyssawki odczepiają się i cała akcja powtarza się. Podczas pełzania czynność serca prawie podwaja swą szybkość, a zwierzę potrzebuje 10–15 minut odpoczynku po względnie niewielkim wysiłku[19].
Większość ośmiornic pływa, wyrzucając strumień wody z płaszcza przez syfon. Siła wywierana na wodę i przyśpieszająca ją przez ujście powoduje odpychanie ośmiornicy w przeciwnym zwrocie[73]. Kierunek zależy od ułożenia syfonu. Podczas tego rodzaju pływania głowa, uniesiona, znajduje się na przedzie, a syfon z tyłu, jednak podczas odrzutu przodują trzewia, syfon kieruje się ku głowie. Ramiona są ciągnięte za głową, często poniżej, blisko ciała. Zwierzę ma wtedy kształt wrzecionowaty. W alternatywnej metodzie pływania niektóre gatunki spłaszczają się grzbietowo-brzusznie z ramionami po bokach, co może być szybsze od zwykłego pływania. Odrzut służy do ucieczki przed niebezpieczeństwem, ale jest fizjologicznie niewydajny, wymaga tak wysokiego ciśnienia w płaszczu, że serce nie może pompować krwi, co skutkuje narastającym niedoborem tlenu[72].
Frędzlikowce nie mają zdolności odrzutu i polegają podczas pływania na swych płetwach. Cechuje je naturalna wyporność, dryfują w wodzie, rozszerzając swe płetwy. Potrafią także kurczyć ramiona i otaczającą je błonę, by wykonywać nagłe ruchy określane po angielsku jako „take-offs”. Inną formą przemieszczania się jest „pompowanie”, obejmujące symetryczne skurcze mięśni w błonie międzyramieniowej wywołujące fale perystaltyczne.
W 2005 odkryto Adopus aculeatus i Amphioctopus marginatus spacerujące na dwóch ramionach podczas naśladowania materii roślinnej[74]. Ten sposób poruszania się umożliwia ośmiornicom przemieszczać się szybko i ujść potencjalnemu drapieżnikowi bez ujawniania się[72]. Badania poświęcone temu zachowaniu przyniosły sugestię, zgodnie z którą dwie najbardziej tylne macki powinny być raczej określane mianem nóg, niż ramion[75]. Przedstawiciele pewnych gatunków potrafią szybko wypełznąć z wody, na przykład przejść z jednego basenu pływowego do drugiego podczas polowań na skorupiaki czy mięczaki bądź też w celu ucieczki przed drapieżnikiem[76][77]. Amphioctopus marginatus chodzi jak na szczudłach, kiedy niesie stos kokosów. Trzyma je od spodu dwoma ramionami, posuwając się do przodu niezgrabnym krokiem pozostałymi, sztywno ustawionymi ramionami[78].
Inteligencja
Ośmiornice są bardzo inteligentne, jednak zakres ich inteligencji i zdolności uczenia się nie zostały dobrze określone[79][80][81][82]. Eksperymenty z udziałem labiryntu i badające rozwiązywanie problemów wykazały obecność pamięci zarówno krótkotrwałej, jak i długotrwałej. Nie wiadomo dokładnie, jak uczenie się wpływa na zachowanie dorosłego osobnika. Młodsze ośmiornice nie uczą się niczego od rodziców, bo ci zapewniają pieczę nad jajami, ale już nie nad wylęgłymi z nich młodymi[51].
W eksperymentach laboratoryjnych ośmiornice można podobno wytrenować w rozróżnianiu odmiennych kształtów i wzorów. Uczą się one przez obserwowanie[83], choć jakość tych doniesień jest kwestionowana[79][80]. Obserwowano ośmiornice podczas zabawy: powtarzały upuszczanie kręcącej się butelki bądź zabawki w swych akwariach i łapały ją[84]. Ośmiornice często wychodzą z akwariów i czasami wchodzą do innych, poszukując pożywienia[76][85][86]. Wchodziły nawet na łodzie rybackie i do ładowni, by zjadać kraby[81]. Amphioctopus marginatus zbiera wyrzucone łupiny orzechów kokosowych i buduje z nich kryjówkę[78]
Jeśli chodzi o odczuwanie bólu, według badań ośmiornice mogą odczuwać ból emocjonalny (psychologiczny) podobnie jak ssaki[87].
Kamuflaż i zmiana barwy
Ośmiornice wykorzystują kamuflaż podczas polowania oraz do ukrywania się przed drapieżnikami. Umożliwiają im to wyspecjalizowane komórki skóry dostosowujące swą barwę, przejrzystość i refleksyjność. Chromatofory zawierają żółte, pomarańczowe, czerwone, brązowe i czarne pigmenty. Większość gatunków dysponuje trzema barwami z tej listy, niektóre dwoma bądź czterema. Inne zmieniające kolor komórki to refleksyjne irydofory i białe leukofory[88]. Zdolność zmiany koloru służy też komunikacji z innymi ośmiornicami, w tym wysyłaniu sygnałów ostrzegawczych[89].
Ośmiornice potrafią tworzyć rozpraszające wzory z falami ciemnej barwy przemieszczającymi się wzdłuż ciała, co po angielsku nazywa się „przelatującymi chmurami”. Mięśnie skórne zmieniają teksturę płaszcza, co polepsza kamuflaż. Płaszcz niektórych gatunków potrafi naśladować kolczasty wygląd glonów. U ogranicza się to do względnie jednorodnych cieni jednej barwy z ograniczoną teksturą. Ośmiornice wiodące dzienny tryb życia w płytkich wodach wykształciły bardziej złożoną skórę niż te nocne czy głębokowodne[89].
Obrona
Prócz ludzi na ośmiornice polują ryby, ptaki morskie, płetwonogie, walenie i inne głowonogi[90]. Ośmiornice zazwyczaj ukrywają się dzięki kamuflażowi i mimikrze. Niektóre cechują się rzucającym się w oczy ubarwieniem ostrzegawczym bądź podejmują zachowanie dejmatyczne[89]. Osobnik może spędzić 40% czasu ukryty w swej norze. Kiedy ktoś się do niej zbliża, ośmiornica może wysunąć swe ramię, by sprawdzić, co się dzieje. W jednym z badań 66% Enteroctopus dolfleini miało blizny, a 50% amputowane ramiona[90]. Niebieskie pierścienie wysoce toksycznej Hapalochlaena są skryte w fałdach mięśniowych, które w razie zagrożenia kurczą się, ukazując opalizujące ostrzeżenie[91]. Pokazy takie są wzmacnianie rozciąganiem ramion, płetw bądź błony międzyramieniowej, przez co zwierzę zdaje się większe i groźniejsze niż w rzeczywistości[92].
Zauważone przez drapieżnika, zazwyczaj próbują ucieczki, mogą jednak odwracać jego uwagę chmurą sepii wyrzucaną z woreczka. Uważa się, że sepia zmniejsza wrażliwość narządu węchu, co utrudnia polowanie drapieżnikom wykorzystującym węch, takim jak rekiny. Chmura sepii pewnych gatunków może sprawiać wrażenie ciała zwierzęcia, wabika, który zamiast ośmiornicy jest atakowany przez drapieżcę[93].
Atakowane, niektóre ośmiornice dokonują autotomii sposobem podobnym do obserwowanego u scynków czy innych jaszczurek odrzucających ogon. Pełzające ramię odwraca uwagę potencjalnego drapieżnika. Pozostawione ramię zachowuje wrażliwość na bodźce i zdolne jest oddalać się od nieprzyjemnych bodźców[94]. Natomiast ośmiornica regeneruje brakujące ramię[95].
Niektóre ośmiornice (na przykład Thaumoctopus mimicus) potrafią wykorzystywać bardzo giętkie ciało oraz możliwość zmiany kolorów do upodabniania się do innych, bardziej niebezpiecznych zwierząt, takich jak Pterois, węże morskie lub węgorzokształtne[96][97].
Patogeny i pasożyty
Choroby i pasożyty ośmiornic zbadano w niewielkim stopniu, choć wiadomo, że głowonogi stanowią żywicieli pośrednich bądź ostatecznych różnych pasożytniczych tasiemców, nicieni i widłonogów. Rozpoznano u nich 150 gatunków pasożytniczych protistów bądź zwierząt[98]. Dicyemidae to rodzina maleńkich robakowatych zwierząt znajdowanych w nerkach wielu gatunków[99]. Pozostaje niejasnym, czy są one pasożytami, czy też może endosymbiontami. Występujące w jelitach żywiciela pierwotniaki, Coccidia z rodzaju Aggregata, mogą być u niego przyczyną ciężkich chorób. Układ odpornościowy ośmiornic ma zdolność odpowiedzi nieswoistej, hemocyty reagują na infekcje poprzez fagocytozę, enkapsulację, infiltrację i aktywność cytotoksyczną, niszcząc w ten sposób bądź izolując patogeny. Hemocyty odgrywają ważną rolę w rozpoznawaniu i eliminacji ciał obcych oraz gojeniu ran. Schwytane osobniki wykazywały większą podatność na patogeny niż żyjące dziko[100]. Gram-ujemna bakteria Vibrio lentus powoduje zmiany i ubytki skórne, a w przypadkach ekstremalnych nawet zgon zwierzęcia[101].
Ewolucja
Filogeneza i zapis kopalny
Głowonogi istnieją od 500 milionów lat. Przodkowie ośmiornic żyli w morzach karbońskich 300 milionów lat temu. Najstarsza znana ośmiornica to Pohlsepia sprzed 296 milionów lat. Zidentyfikowano odciski ośmiu ramion, dwóch oczu i prawdopodobnie woreczka czernidłowego[102]. Ośmiornicę budują głównie tkanki miękkie, co przekłada się na względną rzadkość skamielin. Ośmiornice, mątwy i kałamarnice należą do kladu płaszczoobrosłych, znanego jako głowonogi o miękkim ciele, pozbawione zewnętrznej muszli innych mięczaków, takich jak łodzikowce czy amonity[103]. Ośmiornice mają 8 ramion jak inne płaszczoobrosłe, brakuje im jednak dodatkowych wyspecjalizowanych wyrostków zwanych czułkami, dłuższych i cieńszych, z przyssawkami tylko na pałkowatym końcu[104][105][106]. Wampirzyca piekielna również nie ma czułków, ma za to filamenty zmysłowe[107].
Dwie możliwe filogenezy głowonogów na podstawie badań genetycznych autorstwa Strugnell i in. z 2007 ukazują poniższe kladogramy[108]:
| Cephalopoda |
| ||||||||||||||||||
| Cephalopoda |
| ||||||||||||||||||
Taksonomia
Nazwa naukowa Octopoda została stworzona i nadana rzędowi ośmiornic w 1818 przez angielskiego biologa Williama Elforda Leacha[109], który rok wczesnej zaklasyfikował je jako Octopoida[110]. Rząd składa się z 300 znanych gatunków[111] i dzieli się na dwa podrzędy: ośmiornice właściwe i frędzlikowce. Większość gatunków zalicza się do ośmiornic właściwych, nie ma cirri ani pary płetw frędzlikowców[59]. W dodatku szkielet wewnętrzny Incirrina przyjmuje formę pary sztyletów bądź nie ma wcale[112].
- Rząd Octopoda
 Rekonstrukcja Keuppia levante, wymarłego gatunku z kredy
Rekonstrukcja Keuppia levante, wymarłego gatunku z kredy- Rodzaj †Keuppia (incertae sedis)
- Rodzaj †Palaeoctopus (incertae sedis)
- Rodzaj †Paleocirroteuthis (incertae sedis)
- Rodzaj †Pohlsepia (incertae sedis)
- Rodzaj †Proteroctopus (incertae sedis)
- Rodzaj †Styletoctopus (incertae sedis)
- Podrząd Cirrina
- Rodzina Opisthoteuthidae
- Rodzina Cirroctopodidae
- Rodzina Cirroteuthidae
- Rodzina Stauroteuthidae
- Podrząd Incirrina
- Nadrodzina Octopodoidea
- Rodzina Amphitretidae
- Rodzina Bolitaenidae
- Rodzina Octopodidae
- Rodzaj Enteroctopus
- Rodzaj Octopus
- Rodzina Vitreledonellidae
- Nadrodzina ArgonautoideaArgonauta argo
- Rodzina Alloposidae
- Rodzina Argonautidae
- Rodzina Ocythoidae
- Rodzina Tremoctopodidae
- Nadrodzina Octopodoidea
Edytowanie RNA
U ośmiornic i innych płaszczoobrosłych proces edytowania RNA zachodzi w większym zakresie niż u innych organizmów. Obejmuje ono transformacje nukleotydów transkryptomu i jest związane przede wszystkim z układem nerwowym – dotyczy biosyntezy białek zaangażowanych w pobudliwość i morfologię neuronów. Edytowaniu podlega ponad 60% transkryptów RNA w mózgach płaszczoobrosłych, podczas gdy w przypadku człowieka czy muszki owocowej wartość ta wynosi poniżej 1%. U płaszczoobrosłych w edytowanie RNA zaangażowane są głównie enzymy ADAR, wymagające dużych, dwuniciowych struktur RNA oskrzydlających miejsca edytowania. Zarówno struktura, jak i miejsca edytowania, są w genomie płaszczoobrosłych konserwatywne; częstość mutacji jest w tych miejscach silnie zredukowana. Większa plastyczność transkryptomu skutkuje więc wolniejszą ewolucją genomu. Wysoki poziom edytowania RNA wydaje się nie występować u bardziej pierwotnych głowonogów i innych mięczaków[113][114].
Relacje z człowiekiem

Odniesienia kulturowe
Starożytni ludzie morza znali ośmiornice, o czym świadczą dzieła sztuki. Przykładowo kamienna rzeźba pochodząca z epoki brązu cywilizacji minojskiej Krety z Knossos (1900–1100 p.n.e.) obejmuje przedstawienie rybaka niosącego ośmiornicę[115]. Straszliwe i potężne Gorgony z mitologii greckiej mogły zostać zainspirowane ośmiornicami czy kalmarami. Ośmiornica reprezentuje odciętą głowę Meduzy z dziobem jako wystającymi językiem i zębami oraz ramionami jako wężami[116]. W legendach ludów Europy Północnej występuje Kraken, olbrzymich rozmiarów wieloramienny potwór morski podobno zamieszkujący u wybrzeży Norwegii i Grenlandii i atakujący statki. Karol Linneusz uwzględnił takie stworzenie w pierwszym wydaniu Systema Naturae z 1735 roku pod nazwą Microcosmus[117][118]. Hawajski mit stworzenia stanowi, że współczesny kosmos jest ostatni z szeregu powstających z gruzów poprzednich wszechświatów. Ośmiornica ma w nim być jedyną istotą ocalałą z poprzedniego, obcego świata[119]. W folklorze Ajnów występuje olbrzymi podobny do ośmiornicy potwór Akkorokamui[120].
Walka z ośmiornicą odgrywa znaczącą rolę w powieści Victora Hugo Pracownicy morza (Les Travailleurs de la Mer)[121]. Ian Fleming w opowiadaniu Ośmiorniczka z 1966 roku, wydanym w zbiorze pod tym samym tytułem, czerpał inspirację z Hugo[122]. Nawiązania do tego motywu zawarto w 13. oficjalnym filmie o przygodach Jamesa Bonda, Ośmiorniczka (1983).
Ośmiornice znalazły miejsce w japońskiej sztuce erotycznej, zwanej shunga. Zaliczający się do ukiyo-e (drzeworytów) Sen żony rybaka (Tako to ama, 1814) autorstwa Hokusai przedstawia tytułową amę, bądź żonę rybaka, splecioną w seksualnym uścisku z wielką i małą ośmiornicą[123][124]. Obraz jest prekursorem erotyki macek[125].
Jako gibkie zwierzę wyposażone w liczne ramiona wychodzące z jednego ośrodka, ośmiornica często staje się symbolem silnych i manipulacyjnych organizacji, zazwyczaj w negatywnym kontekście[126].
Zagrożenia

Ośmiornice ogólnie unikają ludzi, ale odnotowano przypadki atakowania człowieka. Przykładowo mierząca 2,4 m ośmiornica olbrzymia, świetnie zakamuflowana, rzuciła się na nurka i starała się wyrwać mu kamerę[127].
Wszystkie gatunki są jadowite, jednak tylko Hapalochlaena dysponują jadem potencjalnie groźnym dla człowieka[128]. Ugryzienia zdarzają się każdego roku w obrębie całego zasięgu występowania tych zwierząt od Australii do wschodniego Indopacyfiku. Gryzą tylko sprowokowane czy niechcący nadepnięte, ukąszenia są niewielkie i zazwyczaj bezbolesne. Jad najprawdopodobniej przy przedłużonym kontakcie przenika przez skórę bez nakłucia. Zawiera tetradotoksynę, wywołującą porażenie przez blokowanie przewodzenia impulsów nerwowych do mięśni. Powoduje to niewydolność oddechową prowadzącą do niedotlenienia OUN i ostatecznie zgon. Nie ma antidotum, ale w przypadku sztucznie utrzymywanego oddychania pacjent zdrowieje w ciągu 24 godzin[129][130]. Odnotowywano też ugryzienia trzymanych w niewoli ośmiornic innych rodzajów. Powodują one obrzęk zanikający w czasie jednego, dwóch dni[131].
Połowy i wykorzystanie kulinarne
Od 1986 do 1995 roku na całym świecie odłowiono ośmiornice w liczbie od 245 320 do 322 999 ton[132]. Światowy szczyt osiągnięto w 2007 roku odłowem o łącznej masie 380 tys. ton, po czym do 2012 nastąpił spadek o jedną dziesiątą[133]. Metody odłowu obejmują pułapki, więcierze, włoki, połowy w dryfie, ataki włócznią, łowienie hakiem i ręką[132]. Ośmiornice są jadane w wielu kulturach i stanowią popularne źródło pokarmu w rejonie Morza Śródziemnego i na wybrzeżach azjatyckich[134][135]. Ramiona i czasami inne części ciała przyrządza się na różne sposoby, często zależne od gatunku i miejsca. W niektórych okolicach na świecie jada się żywe ośmiornice, m.in. w USA[136][137]. Działacze ochrony dobrostanu zwierząt sprzeciwiają się tej praktyce, powołując się na odczuwanie przez ośmiornice bólu[138]. Ośmiornice cechują się wysoką efektywnością wykorzystania paszy, większą niż kurczaki, co daje nadzieję na wydajną akwakulturę ośmiornic[139].
W nauce i technologii
W okresie klasycznym Arystoteles opisał zmianę barwy ośmiornicy dla kamuflażu i sygnalizacji w swej Historia animalium, zwracając uwagę na możliwość dostosowania barwy do koloru otoczenia bądź w razie zagrożenia[140]. Filozof zauważył, że ośmiornica ma hektokotylus, i zasugerował, że może on służyć rozrodowi. Nie wierzono mu aż do XIX wieku. Hektokotylus został opisany w 1829 roku przez francuskiego zoologa Georges'a Cuviera, który uznał go za pasożytniczego robaka i nadał mu nazwę gatunkową Hectocotylus octopodis[141][142]. Inni zoolodzy stwierdzili, że jest to narząd, spermatofor. Niemiecki zoolog Heinrich Müller uważał, że hektokotylus naturalnie odłącza się podczas kopulacji. W 1856 roku duński zoolog Johann Steenstrup wykazał, że narząd ten służy do transferu nasienia i rzadko się odłącza[143].
Ośmiornice dają naukowcom wiele możliwości badawczych, zwłaszcza jeśli chodzi o regenerację ramion, zmianę barwy skóry, inteligentne zachowania związane z rozproszonym układem nerwowym, jak też o 168 rodzajów protokadheryn (ludzie mają ich 58), czyli białek kierujących tworzeniem się połączeń neuronalnych. Zsekwencjonowano genom Octopus bimaculoides, umożliwiając eksplorację adaptacji molekularnych[144]. Ośmiornice wykształciły na drodze konwergencji inteligencję dorównującą ssaczej, dlatego były porównywane do hipotetycznej pozaziemskiej inteligencji[145]. Umiejętność rozwiązywania problemów wraz z ruchliwością i brakiem sztywnej struktury umożliwia im ucieczkę z akwariów publicznych uznawanych za dobrze zabezpieczone[146].
Wysoka inteligencja ośmiornic sprawia, że w niektórych krajach wymienia się je jako zwierzęta laboratoryjne, na których zabiegi chirurgiczne można wykonywać jedynie po znieczuleniu (podobny poziom ochrony zapewniany jest zwykle tylko kręgowcom). W Wielkiej Brytanii od 1993 do 2012 roku ośmiornica pospolita była jedynym bezkręgowcem chronionym przez Animals (Scientific Procedures) Act 1986[147]. W 2012 roku prawo to rozszerzono na wszystkie inne głowonogi[148], zgodnie z dyrektywą Unii Europejskiej[149].
Pewne badania z zakresu robotyki obejmują eksplorację bioniki cech ośmiornic. Ramiona tych zwierząt mogą poruszać się i odbierać bodźce autonomicznie względem OUN. W 2015 roku zespół we Włoszech zbudował roboty o miękkim ciele potrafiące pełzać i pływać, wymagające jedynie minimalnych obliczeń[150]. W 2017 niemiecka firma stworzyła ramię pneumatyczne zaopatrzone w chwytak z miękkiego silikonu z dwoma rzędami przyssawek. Potrafi ono chwytać rozmaite przedmioty (np. metalową rurę, czasopismo czy piłkę), a także napełnić szklankę wodą nalewaną z butelki[151].
Przypisy
- ↑ Octopoda, [w:] Integrated Taxonomic Information System [online] (ang.).
- ↑ Online Etymology Dictionary. Etymonline.com. [dostęp 2014-02-04].
- ↑ Octopus. [w:] Dictionary.reference.com [on-line]. [dostęp 2014-02-04].
- ↑ Henry George Liddell, Robert Scott: ὀκτώπους. [w:] A Greek-English Lexicon [on-line]. Clarendon Press, 1940.
- ↑ Smithsonian National Zoological Park: Giant Pacific Octopus. Nationalzoo.si.edu. [dostęp 2014-02-04]. [zarchiwizowane z tego adresu].
- ↑ Cosgrove, J.A. 1987. Aspects of the Natural History of Octopus dofleini, the Giant Pacific Octopus. MSc Thesis. Department of Biology, University of Victoria (Canada), 101 s.
- ↑ Norman, M. 2000. Cephalopods: A World Guide. ConchBooks, Hackenheim. s. 214.
- ↑ William L. High. The giant Pacific octopus. „Marine Fisheries Review”. 38 (9), s. 17–22, 1976. U.S. National Marine Fisheries Service.
- ↑ S. O’Shea. The giant octopus Haliphron atlanticus (Mollusca: Octopoda) in New Zealand waters. „New Zealand Journal of Zoology”. 31 (1), s. 7–13, 2004. DOI: 10.1080/03014223.2004.9518353.
- ↑ S. O’Shea. Haliphron atlanticus – a giant gelatinous octopus. „Biodiversity Update”. 5, s. 1, 2002.
- ↑ Bradford, Alina: Octopus Facts. Live Science, 2016-07-21. [dostęp 2017-03-26].
- ↑ a b c d e f g h i j k l m Edward E. Ruppert, Richard S. Fox, Robert D. Barnes: Invertebrate Zoology. Cengage Learning, 2008, s. 363–364. ISBN 978-81-315-0104-7.
- ↑ Wells 1978 ↓, s. 11–12.
- ↑ Ruth A. Byrne i inni, Does Octopus vulgaris have preferred arms?, „Journal of Comparative Psychology (American Psychological Association)”, 120 (3), 2006, s. 198–204.
- ↑ John Lloyd, John Mitchinson, The Second Book of General Ignorance, Londyn: Faber and Faber., 2010, ISBN 0-571-27375-0, Cytat: s. 3: As result, marine biologists tend to refer to them as animals with two legs and six arms.
- ↑ a b Mather, Anderson i Wood 2010 ↓, s. 13–15.
- ↑ a b c d Courage 2013 ↓, s. 40–41.
- ↑ J.M. Semmens A G i inni, Understanding octopus growth: patterns, variability and physiology, „Marine and Freshwater Research”, 55, 2004, s. 367, DOI: 10.1071/MF03155.
- ↑ a b Crowfoot, Thomas: Octopuses and Relatives: Locomotion, Crawling. [w:] A Snail’s Odyssey [on-line]. [dostęp 2017-03-19]. [zarchiwizowane z tego adresu (2013-05-22)].
- ↑ I. Zelman, M. Titon, Y. Yekutieli, S. Hanassy i inni. Kinematic decomposition and classification of octopus arm movements. „Frontiers in Computational Neuroscience”, 2013. DOI: 10.3389/fncom.2013.00060. PMID: 23745113. PMCID: PMC3662989.
- ↑ Katherine Harmon Courage, Octopus Arms, Human Tongues Intertwine for Science, Scientific American Blog Network [dostęp 2019-08-24] (ang.).
- ↑
 F. Tramacere, L. Beccai, M. Kuba, A. Gozzi i inni. The morphology and adhesion mechanism of Octopus vulgaris suckers. „PLOS ONE”. 8 (6), s. e65074, 2013. DOI: 10.1371/journal.pone.0065074. PMID: 23750233. PMCID: PMC3672162.
F. Tramacere, L. Beccai, M. Kuba, A. Gozzi i inni. The morphology and adhesion mechanism of Octopus vulgaris suckers. „PLOS ONE”. 8 (6), s. e65074, 2013. DOI: 10.1371/journal.pone.0065074. PMID: 23750233. PMCID: PMC3672162. - ↑ W.M. Kier, A.M. Smith. The structure and adhesive mechanism of octopus suckers. „Integrative and Comparative Biology”. 42 (6), s. 1146–1153, 2002. DOI: 10.1093/icb/42.6.1146. PMID: 21680399.
- ↑ Octopus Senses - Octopus Facts and Information [dostęp 2019-08-24] (ang.).
- ↑ Co widzi mątwa i ośmiornica…?, maxmania.pl, 21 lutego 2012 [dostęp 2019-08-24] (pol.).
- ↑ a b c Wells 1978 ↓, s. 31–35.
- ↑ a b c Courage 2013 ↓, s. 42–43.
- ↑ a b Schmidt-Nielsen, Knut: Animal Physiology: Adaptation and Environment. Cambridge University Press, 1997, s. 117. ISBN 0-521-57098-0.
- ↑ a b Wells 1978 ↓, s. 24–26.
- ↑
 M.J. Wells, J. Wells. The control of ventilatory and cardiac responses to changes in ambient oxygen tension and oxygen demand in Octopus. „The Journal of Experimental Biology”. 198, s. 1717–1727, 1995. PMID: 9319626.
M.J. Wells, J. Wells. The control of ventilatory and cardiac responses to changes in ambient oxygen tension and oxygen demand in Octopus. „The Journal of Experimental Biology”. 198, s. 1717–1727, 1995. PMID: 9319626. - ↑
 J. Wells. Cutaneous respiration in Octopus vulgaris. „The Journal of Experimental Biology”. 199, s. 2477–2483, 1996. PMID: 9320405.
J. Wells. Cutaneous respiration in Octopus vulgaris. „The Journal of Experimental Biology”. 199, s. 2477–2483, 1996. PMID: 9320405. - ↑ a b Wells 1978 ↓, s. 73–79.
- ↑ Boyle, P. R.: Neural Control of Cephalopod Behavior. W: Dennis Willows, A.O.: The Mollusca. T. 8: Neurobiology and Behavior. Academic Press, 2013. ISBN 0-12-751409-0.
- ↑ Wells 1978 ↓, s. 54–56.
- ↑ NOVA: Kings of camouflage. Film Finance Corporation Australia Limited & Kaufmann Productions; WGBH, 2007.
- ↑
 Hochner, B. An Embodied View of Octopus Neurobiology. „Current Biology”. 22 (20), s. R887–R892, 2012. DOI: 10.1016/j.cub.2012.09.001. PMID: 23098601.
Hochner, B. An Embodied View of Octopus Neurobiology. „Current Biology”. 22 (20), s. R887–R892, 2012. DOI: 10.1016/j.cub.2012.09.001. PMID: 23098601. - ↑ Y. Yekutieli, R. Sagiv-Zohar, R. Aharonov, Y. Engel i inni. Dynamic model of the octopus arm. I. Biomechanics of the octopus reaching movement. „J. Neurophysiol.”. 94 (2), s. 1443–1458, 2005. DOI: 10.1152/jn.00684.2004. PMID: 15829594.
- ↑
 L. Zullo, G. Sumbre, C. Agnisola, T. Flash i inni. Nonsomatotopic organization of the higher motor centers in Octopus. „Current Biology”. 19 (19), s. 1632–1636, 2009. DOI: 10.1016/j.cub.2009.07.067. PMID: 19765993.
L. Zullo, G. Sumbre, C. Agnisola, T. Flash i inni. Nonsomatotopic organization of the higher motor centers in Octopus. „Current Biology”. 19 (19), s. 1632–1636, 2009. DOI: 10.1016/j.cub.2009.07.067. PMID: 19765993. - ↑
 G. Kawamura. Color Discrimination Conditioning in Two Octopus Octopus aegina and O. vulgaris. „Nippon Suisan Gakkashi”. 67 (1), s. 35–39, 2001. DOI: 10.2331/suisan.67.35. (jap.).
G. Kawamura. Color Discrimination Conditioning in Two Octopus Octopus aegina and O. vulgaris. „Nippon Suisan Gakkashi”. 67 (1), s. 35–39, 2001. DOI: 10.2331/suisan.67.35. (jap.). - ↑ Vecchione, Michael, Young, Richard E. & Piatkowski, Uwe. Cephalopods of the northern Mid-Atlantic Ridge. „Marine Biology Research”. 6 (1), s. 25–52, 2010. Taylor & Francis. DOI: 10.1080/17451000902810751. (ang.).
- ↑ Matt Walker: The cephalopods can hear you. BBC, 2009-06-15. [dostęp 2013-06-19].
- ↑ Nell Greenfieldboyce: Why This Octopus Isn’t Stuck-Up. [w:] NPR.org [on-line]. 2014-05-15.
- ↑ Wells 1978 ↓, s. 228–244.
- ↑ Mather, Anderson i Wood 2010 ↓, s. 107.
- ↑
 Derby, C. D. Cephalopod Ink: Production, Chemistry, Functions and Applications. „Marine Drugs”. 12 (5), s. 2700–2730, 2014. DOI: 10.3390/md12052700.
Derby, C. D. Cephalopod Ink: Production, Chemistry, Functions and Applications. „Marine Drugs”. 12 (5), s. 2700–2730, 2014. DOI: 10.3390/md12052700. - ↑ a b Finned Deep-sea Octopuses, Grimpoteuthis spp.. MarineBio. [dostęp 2017-12-19].
- ↑ Mather, Anderson i Wood 2010 ↓, s. 147.
- ↑ Martin J. Wells, J. Wells. Optic glands and the state of the testis in Octopus. „Marine Behaviour and Physiology”. 1 (1–4), s. 71–83, 1972. DOI: 10.1080/10236247209386890.
- ↑ R.E. Young, M. Vecchione, K.M. Mangold: Cephalopoda Glossary. [w:] Tree of Life web project [on-line]. 1999.
- ↑ a b Crowfoot, Thomas: Octopuses and Relatives: Reproduction. [w:] A Snail’s Odyssey [on-line]. [dostęp 2017-03-11]. [zarchiwizowane z tego adresu (2017-04-22)].
- ↑ a b c Giant Pacific Octopus (Enteroctopus dofleini) Care Manual. AZA (Association of Zoos and Aquariums) Aquatic Invertebrate Taxonomic Advisory Group in association with AZA Animal Welfare Committee, 2014. s. 74–75. [dostęp 2016-05-31].
- ↑ David Scheel, Giant Octopus: Fact Sheet, Alaska Pacific University [zarchiwizowane z adresu 2012-11-15].
- ↑ Anderson, Roland C., Mather, Jennifer A., Wood, James B.: Octopus: The Ocean’s Intelligent Invertebrate. Timber Press, 2013, s. 147. ISBN 978-1-60469-500-7.
- ↑
 J.W. Forsythe, R.T. Hanlon. A closed marine culture system for rearing Octopus joubini and other large-egged benthic octopods. „Laboratory Animals”. 14 (2), s. 137–142, 1980. DOI: 10.1258/002367780780942737.
J.W. Forsythe, R.T. Hanlon. A closed marine culture system for rearing Octopus joubini and other large-egged benthic octopods. „Laboratory Animals”. 14 (2), s. 137–142, 1980. DOI: 10.1258/002367780780942737. - ↑ Octopus Fact Sheet. World Animal Foundation. [dostęp 2017-03-12]. [zarchiwizowane z tego adresu (2016-06-10)].
- ↑ Simon, Matt: Absurd Creature of the Week: The Beautiful Octopus Whose Sex Is All About Dismemberment. [w:] Wired: Science [on-line]. 2015-01-16. [dostęp 2017-05-20].
- ↑ Roland C. Anderson, James B. Wood, Ruth A. Byrne. Octopus Senescence: The Beginning of the End. „Journal of Applied Animal Welfare Science”. 5 (4), s. 275–283, 2002. DOI: 10.1207/S15327604JAWS0504_02.
- ↑ Jerome Wodinsky. Hormonal Inhibition of Feeding and Death in Octopus: Control by Optic Gland Secretion. „Science”. 198 (4320), s. 948–951, 1977. DOI: 10.1126/science.198.4320.948. PMID: 17787564.
- ↑ a b Marshall Cavendish Corporation: Encyclopedia of the Aquatic World. Marshall Cavendish, 2004, s. 764. ISBN 978-0-7614-7424-1.
- ↑ Alan J. Jamieson, Michael Vecchione, First in situ observation of Cephalopoda at hadal depths (Octopoda: Opisthoteuthidae: Grimpoteuthis sp.), „Marine Biology”, 167 (6), 2020, s. 82, DOI: 10.1007/s00227-020-03701-1, ISSN 0025-3162 [dostęp 2021-01-06] (ang.).
- ↑ Norman, Mark: Ask an expert: Are there any freshwater cephalopods?. ABC Science, 2013-01-16. [dostęp 2017-03-26].
- ↑ Patricia Edmonds. What’s Odd About That Octopus? It’s Mating Beak to Beak. „National Geographic”, April 2017.
- ↑ D. Scheel. A second site occupied by Octopus tetricus at high densities, with notes on their ecology and behavior. „Marine and Freshwater Behaviour and Physiology”, 2017. DOI: 10.1080/10236244.2017.1369851.
- ↑ Goldman, Jason G: How do octopuses navigate?. [w:] Scientific American [on-line]. 2012-05-24. [dostęp 2017-06-08].
- ↑ Courage 2013 ↓, s. 45–46.
- ↑ a b Crowfoot, Thomas: Octopuses and Relatives: Feeding, diets and growth. [w:] A Snail’s Odyssey [on-line]. [dostęp 2017-03-13]. [zarchiwizowane z tego adresu (2018-07-06)].
- ↑ a b Maggy Wassilieff, Steve O’Shea: Octopus and squid – Feeding and predation. [w:] Te Ara – the Encyclopedia of New Zealand [on-line]. 2009-03-02.
- ↑ a b Wells 1978 ↓, s. 74–75.
- ↑
 Jerome Wodinsky. Penetration of the Shell and Feeding on Gastropods by Octopus. „American Zoologist”. 9 (3), s. 997–1010, 1969. DOI: 10.1093/icb/9.3.997.
Jerome Wodinsky. Penetration of the Shell and Feeding on Gastropods by Octopus. „American Zoologist”. 9 (3), s. 997–1010, 1969. DOI: 10.1093/icb/9.3.997. - ↑ Crowfoot, Thomas: Octopuses and Relatives: Prey handling and drilling. [w:] A Snail’s Odyssey [on-line]. [dostęp 2017-03-21]. [zarchiwizowane z tego adresu (2018-07-11)].
- ↑ S. Johnsen, E.J. Balser, E.C. Fisher, E.A. Widder. Bioluminescence in the deep-sea cirrate octopod Stauroteuthis syrtensis Verrill (Mollusca: Cephalopoda). „The Biological Bulletin”. 197 (1), s. 26–39, 1999. DOI: 10.2307/1542994.
- ↑ a b c
 Christine L. Huffard. Locomotion by Abdopus aculeatus (Cephalopoda: Octopodidae): walking the line between primary and secondary defenses. „Journal of Experimental Biology”. 209, s. 3697–3707, 2006. DOI: 10.1242/jeb.02435. PMID: 16985187.
Christine L. Huffard. Locomotion by Abdopus aculeatus (Cephalopoda: Octopodidae): walking the line between primary and secondary defenses. „Journal of Experimental Biology”. 209, s. 3697–3707, 2006. DOI: 10.1242/jeb.02435. PMID: 16985187. - ↑ I. Kassim, L. Phee, W.S. Ng, F. Gong i inni. Locomotion techniques for robotic colonoscopy. „IEEE Engineering in Medicine and Biology Society”. 25 (3), s. 40–56, 2006. DOI: 10.1109/MEMB.2006.1636351.
- ↑ Christine L. Huffard, Farnis Boneka, Robert J. Full, Underwater bipedal locomotion by octopuses in disguise, „Science”, 307 (5717), 2005, s. 1927, DOI: 10.1126/science.1109616, PMID: 15790846.
- ↑ Octopuses have only six arms, the other two are actually legs!. highbeam.com. [zarchiwizowane z tego adresu (2013-06-02)]. Hindustan Times, 13-08-2008.
- ↑ a b James B. Wood, Roland C. Anderson. Interspecific Evaluation of Octopus Escape Behavior. „Journal of Applied Animal Welfare Science”. 7 (2), s. 95–106, 2004. Lawrence Erlbaum Associates. DOI: 10.1207/s15327604jaws0702_2. PMID: 15234886.
- ↑ Katherine Harmon: Land-Walking Octopus Explained. [w:] Octopus Chronicles [on-line]. Scientific American, 24 November 2011. [dostęp 2011-11-24].
- ↑ a b
 J.K. Finn, T. Tregenza, M.D. Norman. Defensive tool use in a coconut-carrying octopus. „Current Biology”. 19 (23), s. R1069–R1070, 2009. DOI: 10.1016/j.cub.2009.10.052. PMID: 20064403.
J.K. Finn, T. Tregenza, M.D. Norman. Defensive tool use in a coconut-carrying octopus. „Current Biology”. 19 (23), s. R1069–R1070, 2009. DOI: 10.1016/j.cub.2009.10.052. PMID: 20064403. - ↑ a b Garry Hamilton: What is this octopus thinking?. [zarchiwizowane z tego adresu (7-03-2012)].
- ↑ a b Doug Stewart. Armed but not dangerous: Is the octopus really the invertebrate intellect of the sea. „National Wildlife”. 35 (2), 1997.
- ↑ a b Giant Octopus – Mighty but Secretive Denizen of the Deep. Web.archive.org, 2008. [dostęp 2014-02-04]. [zarchiwizowane z tego adresu (25 August 2012)].
- ↑ Carl Zimmer: How Smart is the Octopus?. Slate.com, 2008-06-23.
- ↑ Octopus intelligence: Jar opening. BBC News, 2003-02-25. [dostęp 2014-02-04].
- ↑ J.A. Mather, R.C. Anderson: What behavior can we expect of octopuses?. The Cephalopod Page, 1998.
- ↑ V: The octopus out of water. W: Henry Lee: Aquarium Notes – The Octopus; or, the „devil-fish” of fiction and of fact. London: Chapman and Hall, 1875, s. 38–39. OCLC 1544491. Cytat: The marauding rascal had occasionally issued from the water in his tank, and clambered up the rocks, and over the wall into the next one; there he had helped himself to a young lump-fish, and, having devoured it, returned demurely to his own quarters by the same route, with well-filled stomach and contented mind..
- ↑ Eleanor Ainge Roy: The great escape: Inky the octopus legs it to freedom from aquarium. [w:] The Guardian (Australia) [on-line]. 2016-03-14.
- ↑ Robyn J. Crook, Behavioral and neurophysiological evidence suggests affective pain experience in octopus, „iScience”, 24 (3), 2021, DOI: 10.1016/j.isci.2021.102229, ISSN 2589-0042, PMID: 33733076 [dostęp 2021-04-06] (ang.).
- ↑ Nadia Meyers: Tales from the Cryptic: The Common Atlantic Octopus. Southeastern Regional Taxonomic Centre. [dostęp 2006-06-27].
- ↑ a b c Mather, Anderson i Wood 2010 ↓, s. 90–97.
- ↑ a b Crowfoot, Thomas: Octopuses and Relatives: Predators and Defenses. [w:] A Snail’s Odyssey [on-line]. [dostęp 2017-03-13]. [zarchiwizowane z tego adresu (2018-07-13)].
- ↑
 L.M. Mäthger, G.R. Bell, A.M. Kuzirian, J.J. Allen i inni. How does the blue-ringed octopus (Hapalochlaena lunulata) flash its blue rings?. „Journal of Experimental Biology”. 215 (21), s. 3752–3757, 2012. DOI: 10.1242/jeb.076869. PMID: 23053367.
L.M. Mäthger, G.R. Bell, A.M. Kuzirian, J.J. Allen i inni. How does the blue-ringed octopus (Hapalochlaena lunulata) flash its blue rings?. „Journal of Experimental Biology”. 215 (21), s. 3752–3757, 2012. DOI: 10.1242/jeb.076869. PMID: 23053367. - ↑ Hanlon, R. T., Messenger, J. B.: Cephalopod Behaviour. Cambridge University Press, 1998, s. 80–81. ISBN 978-0-521-64583-6.
- ↑ R.L. Caldwell. An Observation of Inking Behavior Protecting Adult Octopus bocki from Predation by Green Turtle (Chelonia mydas) Hatchlings. „Pacific Science”. 59 (1), s. 69–72, 2005. DOI: 10.1353/psc.2005.0004.
- ↑ Katherine Harmon: Even Severed Octopus Arms Have Smart Moves. [w:] Octopus Chronicles [on-line]. Scientific American, 2013.
- ↑ Mather, Anderson i Wood 2010 ↓, s. 85.
- ↑
 M.D. Norman, J. Finn, T. Tregenza. Dynamic mimicry in an Indo-Malayan octopus. „Proceedings of the Royal Society”. 268 (1478), s. 1755–1758, 2001. DOI: 10.1098/rspb.2001.1708. PMID: 11522192. PMCID: PMC1088805.
M.D. Norman, J. Finn, T. Tregenza. Dynamic mimicry in an Indo-Malayan octopus. „Proceedings of the Royal Society”. 268 (1478), s. 1755–1758, 2001. DOI: 10.1098/rspb.2001.1708. PMID: 11522192. PMCID: PMC1088805. - ↑ Norman M.D., The ‘Mimic Octopus’ (''Thaumoctopus mimicus'' n. gen. et sp.), a new octopus from the tropical Indo-West Pacific (Cephalopoda: Octopodidae), „Molluscan Research”, 2, 25, 2005, s. 57–70.
- ↑ Santiago Pascal, Camino Gestal, J. Estevez, Christian Andrés Arias. Parasites in commercially-exploited cephalopods (Mollusca, Cephalopoda) in Spain: An updated perspective. „Aquaculture”. 142, s. 1–10, 1996. DOI: 10.1016/0044-8486(96)01254-9.
- ↑
 Hidetaka Furuya, Kazuhiko Tsuneki. Biology of Dicyemid Mesozoans. „Zoological Science”. 20 (5), s. 519–532, 2003. DOI: 10.2108/zsj.20.519. PMID: 12777824.
Hidetaka Furuya, Kazuhiko Tsuneki. Biology of Dicyemid Mesozoans. „Zoological Science”. 20 (5), s. 519–532, 2003. DOI: 10.2108/zsj.20.519. PMID: 12777824. - ↑ Sheila Castellanos-Martínez, Camino Gestal. Pathogens and immune response of cephalopods. „Journal of Experimental Marine Biology and Ecology”. 447, s. 14–22, 2013. DOI: 10.1016/j.jembe.2013.02.007.
- ↑ R. Farto, S.P. Armada, M. Montes, J.A. Guisande i inni. Vibrio lentus associated with diseased wild octopus (Octopus vulgaris). „Journal of Invertebrate Pathology”. 83 (2), s. 149–156, 2003. DOI: 10.1016/S0022-2011(03)00067-3.
- ↑ Courage 2013 ↓, s. 4.
- ↑ A Broad Brush History of the Cephalopoda. The Cephalopod Group. [dostęp 2017-03-27].
- ↑ R.E. Young, M. Vecchione, K.M. Mangold: Cephalopoda Glossary. Tree of Life web project, 1999. [dostęp 2017-05-30].
- ↑ Octopuses & Squids. Vancouver Aquarium. [dostęp 2017-05-29].
- ↑ Norman, M.: Cephalopods: A World Guide. ConchBooks, 2000, s. 15. ISBN 978-3-925919-32-9.
- ↑ Seibel, B: Vampyroteuthis infernalis, Deep-sea Vampire squid. The Cephalopod Page. [dostęp 2017-05-31].
- ↑
 J. Strugnell, M.K. Nishiguchi. Molecular phylogeny of coleoid cephalopods (Mollusca: Cephalopoda) inferred from three mitochondrial and six nuclear loci: a comparison of alignment, implied alignment and analysis methods. „Journal of Molluscan Studies”. 73 (4), s. 399–410, 2007. DOI: 10.1093/mollus/eym038.
J. Strugnell, M.K. Nishiguchi. Molecular phylogeny of coleoid cephalopods (Mollusca: Cephalopoda) inferred from three mitochondrial and six nuclear loci: a comparison of alignment, implied alignment and analysis methods. „Journal of Molluscan Studies”. 73 (4), s. 399–410, 2007. DOI: 10.1093/mollus/eym038. - ↑ Gofas, S: Octopoda. 2009. [dostęp 2018-01-14].
- ↑ Coleoidea – Recent cephalopods. (ang.).
- ↑ Mather, Anderson i Wood 2010 ↓, s. 145.
- ↑
 D. Fuchs, C. Ifrim, W. Stinnesbeck, A new ''Palaeoctopus'' (Cephalopoda: Coleoidea) from the Late Cretaceous of Vallecillo, north-eastern Mexico, and implications for the evolution of Octopoda, wyd. 5, t. 51, Palaeontology, 2008, s. 1129–1139, DOI: 10.1111/j.1475-4983.2008.00797.x.
D. Fuchs, C. Ifrim, W. Stinnesbeck, A new ''Palaeoctopus'' (Cephalopoda: Coleoidea) from the Late Cretaceous of Vallecillo, north-eastern Mexico, and implications for the evolution of Octopoda, wyd. 5, t. 51, Palaeontology, 2008, s. 1129–1139, DOI: 10.1111/j.1475-4983.2008.00797.x. - ↑ Courage 2013 ↓, s. 46–49.
- ↑ Noa Liscovitch-Brauer i inni, Trade-off between Transcriptome Plasticity and Genome Evolution in Cephalopods, „Cell”, 169 (2), 2017, s. 191–202, DOI: 10.1016/j.cell.2017.03.025, PMID: 28388405.
- ↑ C. Michael Hogan: Knossos fieldnotes. The Modern Antiquarian, 2007.
- ↑ Stephen R. Wilk: Medusa: Solving the Mystery of the Gorgon. Oxford University Press, 2000. ISBN 0-19-988773-X.
- ↑ Karol Linneusz: Caroli Linnaei Systema naturae sistens regna tria naturae. s. 82.
- ↑ Edward Smedley, Hugh James Rose, Henry John Rose: Encyclopaedia Metropolitana, Or, Universal Dictionary of Knowledge: Comprising the Twofold Advantage of a Philosophical and an Alphabetical Arrangement, with Appropriate Engravings. B. Fellowes, 1845, s. 255–258.
- ↑ Roland Burrage Dixon: Oceanic. T. 9. Marshall Jones Company, 1916, s. 2n, seria: The Mythology of All Races.
- ↑ John Batchelor: The Ainu and Their Folklore. London: The Religious Tract Society, 1901.
- ↑ Octopus. W: Hugh Chisholm: Encyclopædia Britannica. Cambridge University Press, 1911.
- ↑ Gerard Cohen-Vrignaud. On Octopussies, or the Anatomy of Female Power. „differences”. 23 (2), s. 32–61, 2012. DOI: 10.1215/10407391-1533520.
- ↑ Sointu Fritze, Saara Suojoki: Forbidden Images: Erotic Art from Japan’s Edo Period. Helsingin kaupungin taidemuseo, 2000, s. 23–28. ISBN 978-951-8965-54-4. (fiń.).
- ↑ Chris Uhlenbeck, Margarita Winkel, Ellis Tinios, Amy Reigle Newland: Japanese Erotic Fantasies: Sexual Imagery of the Edo Period. Hotei, 2005, s. 161. ISBN 90-74822-66-5.
- ↑ Holger Briel: Mark Berninger, Jochen Ecke, Gideon Haberkorn: Comics As a Nexus of Cultures: Essays on the Interplay of Media, Disciplines. McFarland, 2010, s. 203. ISBN 978-0-7864-3987-4.
- ↑ S. Smith: Why Mark Zuckerberg Octopus Cartoon Evokes 'Nazi Propaganda,' German Paper Apologizes. iMediaEthics, 2010-02-26. [dostęp 2017-05-31].
- ↑ Philip Ross: 8-Foot Octopus Wrestles Diver Off California Coast, Rare Encounter Caught on Camera. [w:] International Business Times [on-line]. 2014-02-18.
- ↑ Tentacles of venom: new study reveals all octopuses are venomous. University of Melbourne, 2009.
- ↑ Blue-ringed Octopuses, Hapalochlaena maculosa. The MarineBio Conservation Society. [dostęp 2017-03-12].
- ↑ Roy Caldwell: What makes blue-rings so deadly? Blue-ringed octopus have tetrodotoxin. The Cephalopod Page. [dostęp 2017-03-12].
- ↑ Wells 1978 ↓, s. 68.
- ↑ a b G.E. Gillespie, G. Parker, J. Morrison: A Review of Octopus Fisheries Biology and British Columbia Octopus Fisheries. Canadian Stock Assessment Secretariat, 1998.
- ↑ S. Rocliffe, A. Harris: The status of octopus fisheries in the Western Indian Ocean. 2016. [dostęp 2017-06-18].
- ↑ Cushman, Abi: Common octopus. [w:] Animal fact guide [on-line]. 2014.
- ↑ Giant Pacific octopus. Monterey Bay Aquarium, 2017. [dostęp 2017-12-06]. [zarchiwizowane z tego adresu (2018-07-04)].
- ↑ L. Eriksen: Live and let dine. [w:] The Guardian [on-line]. 10 November 2010. [dostęp 2015-03-15].
- ↑ Silvia Killingsworth: Why not eat octopus?. The New Yorker, 3 October 2014. [dostęp 2016-03-15].
- ↑ M. Ferrier: Macho foodies in New York develop a taste for notoriety. [w:] The Guardian [on-line]. 2010-05-30. [dostęp 2015-03-15].
- ↑ Martin Wells. Cephalopods do it differently. „New Scientist”. 100 (1382), s. 333–334, 1983. Reed Business Information. ISSN 0262-4079.
- ↑ Arystoteles (ok. 350 p.n.e.). Historia animalium. IX, 622a: 2–10. za Borrelli, Luciana; Gherardi, Francesca; Fiorito, Graziano (2006). A catalogue of body patterning in Cephalopoda. Firenze University Press. ISBN 978-88-8453-377-7. Abstract.
- ↑ Armand Marie Leroi: The Lagoon: How Aristotle Invented Science. Bloomsbury, 2014, s. 71–72. ISBN 978-1-4088-3622-4.
- ↑ The Cephalopoda. University of California Museum of Paleontology. [dostęp 2017-03-27].
- ↑ T. Mann: Spermatophores: Development, Structure, Biochemical Attributes and Role in the Transfer of Spermatozoa 8. Springer, 2012, s. 28. ISBN 978-3-642-82308-4.
- ↑ Emily Singer: Biologists Search for New Model Organisms. Quanta Magazine, 2016-06-26.
- ↑ Baer, Drake: Octopuses Are 'the Closest We Will Come to Meeting an Intelligent Alien'. Science of Us, 2016. [dostęp 2017-03-26].
- ↑ Karin Brulliard: Octopus slips out of aquarium tank, crawls across floor, escapes down pipe to ocean. The Washington Post, 2016-03-13. [dostęp 2017-02-20].
- ↑ The Animals (Scientific Procedures) Act (Amendment) Order 1993. The National Archives. [dostęp 2015-02-18].
- ↑ The Animals (Scientific Procedures) Act 1986 Amendment Regulations 2012. The National Archives. [dostęp 2015-02-18].
- ↑ Directive 2010/63/EU of the European Parliament and of the Council. Official Journal of the European Union. [dostęp 2015-02-18].
- ↑ Octopus-Inspired Robots Can Grasp, Crawl, and Swim. IEEE Spectrum, 2015-03-05.
- ↑ Matt Burgess: This robotic octopus tentacle isn’t creepy at all. Wired, 2017-03-27.
Bibliografia
- M.J. Wells: Octopus, Physiology and Behaviour of an Advanced Invertebrate. Springer Science & Business Media, 1978. ISBN 978-94-017-2470-8.
- K.H. Courage: Octopus!, The Most Mysterious Creature in the Sea. Penguin Group, 2013. ISBN 978-0-698-13767-7.
- J.A. Mather, R.C. Anderson, J.B. Wood: Octopus: The Ocean’s Intelligent Invertebrate. Timber Press, 2010. ISBN 978-1-60469-067-5.
Media użyte na tej stronie
Autor: (of code) -xfi-, Licencja: CC BY-SA 3.0
The Wikispecies logo created by Zephram Stark based on a concept design by Jeremykemp.
Tremoctopus violaceus
Zooplankton. Octopus.
Pen and wash drawing by malacologist Pierre Dénys de Montfort, 1801, from the descriptions of French sailors reportedly attacked by such a creature off the coast of Angola.
Autor: Fernando Losada Rodríguez, Licencja: CC BY-SA 4.0
Octopus vulgaris (Octopus) in Sala Maremagnum of Aquarium Finisterrae, in A Coruña, Galicia, Spain.
Octopus vulgaris
"Dumbo" deep sea cirrate octopus, likely Opisthoteuthis californiana. This type of octopus has muscular lateral fins to propel it.
Archaeological Museum in Herakleion. Minoan clay bottle showing an Octopus ( 1500 B.C. )
© Hans Hillewaert, CC BY-SA 4.0
Common squid from the Belgian continental shelf. Picture taken in the lab on board of the RV Belgica, of a live specimen to preserve colour and structure of chromophores.
Mantle: length= 138 mm, width= 39 mm.
Autor: Parent Géry, Licencja: CC BY-SA 3.0
Octopus vulgaris Cuvier, 1798 - Banyuls-sur-Mer : 09/81
"One of the rare finned octopods known as "Dumbos" collected on the summer 2009 MAR-ECO cruise."
Autor: Tomomori, Licencja: CC BY-SA 3.0
North Pacific Giant Octopus in Echizen Matsushima Aquarium, Japan (Enteroctopus dofleini)
Eye of common octopus. U. S. Virgin Islands, Coki Beach, St. Thomas. 2004.
Official patch for NROL-39, a 2013 US government satellite launch
Schematic lateral aspect of octopod features
Autor: prilfish (Silke Baron), Licencja: CC BY 2.0
Reef octopus (Octopus cyanea), also known as the big blue octopus, day octopus and Cyane's octopus. Filmed in the Red Sea.
Autor: Brocken Inaglory, Licencja: CC BY-SA 3.0
Octopus cyanea in Kona, Hawaii
Autor: User:MatthiasKabel, Licencja: CC BY 2.5
Octopus opening a container with a screw cap. Photographed at "Haus der Natur", Salzburg, Austria
(c) Bernd Hofmann at de.wikipedia, CC BY-SA 2.0
Female Argonauta argo with severely damaged eggcase and eggs, encountered at a depth of about 20 cm in a cove at the southern coast of Turkey.
Autor: Jens Petersen, Licencja: CC BY 2.5
Image of a Greater blue-ringed octopus. Hapalochlaena lunulata. Taken at Tasik Ria, North Sulawesi, Indonesia.
Cirroteuthis muelleri
Autor:
SUBnormali Team
Original uploader was Yoruno at it.wikipedia, Licencja: CC BY-SA 3.0it:Octopus macropus
(c) Silke Baron, CC BY 2.0
Veined Octopus - Amphioctopus marginatus eating a Crab.
Autor: Smokeybjb, Licencja: CC BY-SA 3.0
Life restoration of Keuppia levante.
- Based on photograph and restoration found here.