Potas
| – ← potas → wapń | |||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | |||||||||||||||||||||||||||||||||||||||||||||||||
| srebrzystobiały | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
Widmo emisyjne potasu | |||||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwa, symbol, l.a. | potas, K, 19 | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grupa, okres, blok | |||||||||||||||||||||||||||||||||||||||||||||||||
| Stopień utlenienia | I | ||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości metaliczne | |||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości tlenków | |||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa | |||||||||||||||||||||||||||||||||||||||||||||||||
| Stan skupienia | stały | ||||||||||||||||||||||||||||||||||||||||||||||||
| Gęstość | 856 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura topnienia | 63,5 °C[1] | ||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | 759 °C[1] | ||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą warunków normalnych (0 °C, 1013,25 hPa) | |||||||||||||||||||||||||||||||||||||||||||||||||
Potas (K, łac. kalium) – pierwiastek chemiczny z grupy metali alkalicznych o liczbie atomowej 19.
Odkrycie
Potas odkrył i wyodrębnił w 1807 roku Humphry Davy poprzez elektrolizę wodorotlenku potasu[6]. Polską nazwę zaproponował Filip Walter.
Występowanie, izotopy
Głównymi minerałami są sylwin, sylwinit, karnalit, kainit, langbeinit i różne glinokrzemiany.
Trwałe są izotopy 39
K oraz 41
K. Ważnym nietrwałym izotopem jest słabo promieniotwórczy 40
K, z którego, zależnie od sposobu przemiany, powstaje 40
Ar lub 40
Ca. Przemiana w argon jest wykorzystywana w datowaniu skał i minerałów metodą potasowo-argonową.
Charakterystyka
Potas jest bardzo miękkim metalem. Można go kroić nożem, niczym ser. Jest bardzo aktywnym pierwiastkiem, potencjał standardowy układu K+
/K wynosi −2,93 V. W kontakcie z wodą i kwasami zapala się, często wybuchowo. Reaguje z alkoholami, wypierając z nich wodór i tworząc alkoholany. O ile jego powierzchnia nie jest spasywowana (na powietrzu pokrywa się warstwą nadtlenku K
2O
2), w kontakcie z powietrzem może się zapalić. Przechowuje się go w nafcie lub oleju parafinowym (najlepiej pod warstwą argonu).
Ważnymi związkami potasu są tlenek K
2O, nadtlenek K
2O
2 i wodorotlenek KOH, będący bardzo silną zasadą, oraz wiele soli. Prawie wszystkie sole potasu są dobrze rozpuszczalne w wodzie. Do trudno rozpuszczalnych soli potasu należą: nadchloran KClO
4, heksachloroplatynian(IV) K
2[PtCl
6] oraz wodorowinian KHC
4H
4O
6. Potas tworzy także wodorek. Spalany w nadmiarze tlenu tworzy żółty ponadtlenek KO
2, a w ozonie pomarańczowy ozonek KO
3. Ważnym odczynnikiem chemicznym jest nadmanganian potasu KMnO
4.
Potas, podobnie jak sód, wykazuje chemiluminescencję – podczas powolnego utleniania tlenem atmosferycznym występuje delikatne świecenie[7].
Kationy K+
należą do V grupy i barwią płomień na kolor różowo-fioletowy.
Znaczenie biologiczne
- bierze udział w przewodzeniu impulsów przez neuron
- podwyższa stopień uwodnienia koloidów komórkowych
- stanowi aktywator wielu enzymów
Niedobór u człowieka powoduje:
- osłabienie organizmu
- zmniejszenie kurczliwości mięśnia sercowego
- osłabienie mięśni szkieletowych i gładkich
Niedobór u roślin powoduje:
Kationy potasu są głównymi jonami wewnątrzkomórkowymi, koniecznymi do utrzymania potencjału czynnościowego błon komórkowych (patrz: znaczenie biologiczne pierwiastków).
Uwagi
- ↑ Podana wartość stanowi przybliżoną standardową względną masę atomową (ang. abridged standard atomic weight) publikowaną wraz ze standardową względną masą atomową, która wynosi 39,0983 ± 0,0001.
Przypisy
- ↑ a b David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 4-27, ISBN 978-1-4200-9084-0 (ang.).
- ↑ potassium (ang.) w wykazie klasyfikacji i oznakowania Europejskiej Agencji Chemikaliów. [dostęp 2015-04-10].
- ↑ Potassium (nr 244856) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Stanów Zjednoczonych. [dostęp 2011-09-30]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Thomas Prohaska i inni, Standard atomic weights of the elements 2021 (IUPAC Technical Report), „Pure and Applied Chemistry”, 94 (5), 2021, s. 573–600, DOI: 10.1515/pac-2019-0603 (ang.).
- ↑ Potas (nr 244856) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Polski. [dostęp 2011-09-30]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Ignacy Eichstaedt: Księga pierwiastków. Warszawa: Wiedza Powszechna, 1973, s. 132. OCLC 839118859.
- ↑ Marek Ples: Chemiluminescencja metalicznego sodu (pol.). Weird science. [dostęp 2014-10-20].
Bibliografia
- Jerzy Minczewski, Zygmunt Marczenko, Chemia analityczna – 1 podstawy teoretyczne i analiza jakościowa, Warszawa: PWN, 2001, ISBN 83-01-13498-4, ISBN 83-01-13499-2, OCLC 749313943.
Media użyte na tej stronie
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Spectrum of K, 600lpmm
Autor: Maxim Bilovitskiy, Licencja: CC BY-SA 4.0
I put about 0,1 gram of 98% potassium metal in water. Potassium reacts with water very vigorously, producing hydrogen gas and potassium hydroxide.
Autor:
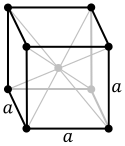
Body-centered cubic crystal structure
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.