Prażenie (technologia chemiczna)
Prażenie – ogrzewanie substancji stałych w wysokiej temperaturze, niższej od ich temperatury topnienia, w celu spowodowania przemian fizycznych lub chemicznych.
Rodzaje procesów prażenia
Rozróżnia się prażenie:
- utleniające, prowadzone w obecności utleniaczy, np. tlenu z powietrza
- redukujące, prowadzone w obecności reduktorów, np. węgla, tlenku węgla
- pirolityczne, prowadzone w atmosferze gazu obojętnego bez obecności środków redukujących i utleniających
- kalcynujące, rozkładające substancję z wydzieleniem różnych gazów, np. kalcynacja wodorowęglanu sodu:
- 2 NaHCO3 → Na2CO3 + H2O↑ + CO2↑.
W chemicznej analizie wagowej i mikroanalizie prażenie osadu, zwykle z udziałem silnych utleniaczy, ma na celu doprowadzenie go do postaci czystego tlenku określonego pierwiastka, na podstawie czego można ustalić zawartość tego pierwiastka w wyjściowej substancji. Na przykład prażenie związków krzemoorganicznych prowadzi się z użyciem kwasu siarkowego, w wyniku czego wszystkie grupy organiczne przyłączone do krzemu przechodzą w tlenki węgla i siarczki, które odparowują, zaś pozostałość stanowi czysta krzemionka. Znając masę wyjściowego związku i ważąc otrzymaną krzemionkę, można ustalić zawartość krzemu w tym związku.
W dużej skali produkcyjnej proces prażenia stosuje się do przetwarzania surowców mineralnych i produktów rolnych i prowadzi w piecach przemysłowych. Można tu wymienić[1][2]:
- przeróbkę węgla kamiennego – koksowanie i wytlewanie
- kalcynowanie kamienia wapiennego w wapiennikach
- przeróbkę rud metali (pirytu, sfalerytu, galmanu, galeny, chalkozynu, chalkopirytu) w piecach zwanych prażakami (znajdujących się w prażalniach)
- otrzymywania tłuszczów roślinnych ze zmiażdżonych nasion roślin oleistych w wyniku prażenia z równoczesnym nawilżaniem i mieszaniem (w tak zwanych prażniach)
- otrzymywania dekstryn z wysuszonego i zakwaszonego krochmalu.
Prażenie w metalurgii (przykład)
Proces prażenia jest stosowany w metalurgii w różnych etapach złożonego procesu hutniczego, na przykład w czasie operacji wstępnej obróbki surowców mineralnych (rud) oraz w czasie zasadniczego przetwarzania chemicznego.
- Przykłady obróbki wstępnej
Wstępna obróbka surowców może polegać na prażeniu do spieczenia. Jest to proces nadtapiania powierzchniowej części drobnych ziaren rudy (np. zmielonej w czasie wzbogacania), co powoduje ich zlepianie się w pożądanym stopniu. W hutnictwie aluminium wstępne prażenie boksytu powoduje dodatkowo rozkład zawartych w rudzie substancji organicznych, co ułatwia ekstrakcję w procesie Bayera[3].
Nadtapianie bez aglomeracji jest korzystne również w innych procesach produkcyjnych, na przykład w czasie otrzymywania kwasu fosforowego metodą ekstrakcyjną (wstępne prażenie fosforytów ogranicza przechodzenie do roztworu tlenków żelaza i glinu)[3].
Prażenie wstępne, na przykład prażenie do spieczenia, jest prowadzone za pomocą, między innymi, taśmowych aparatów spiekalnych Dwighta-Lloyda (taśma spiekalnicza). Konstrukcja tych aparatów jest podobna do konstrukcji rusztów łańcuchowych, w których strumień powietrza przepływa w odwróconym kierunku: z góry w dół. Prażony materiał (lub jego mieszanina z paliwem) ulega zapłonowi po szybkim przesunięciu pod palnikiem; po opuszczeniu taśmy jest sortowany na sitach. Frakcja drobna jest zawracana do strefy prażenia[3][5].
- Przykład metalurgii cyny
Jednym z licznych przykładów zastosowania prażenia w metalurgii jest proces produkcji cyny z rud, w których skład wchodzą tlenki żelaza i innych metali oraz niewielkie ilości kasyterytu (SnO2, minerał zawierający 79% cyny). Jednym z etapów złożonego technologicznego procesu uzyskiwania cyny metalicznej jest w tym przypadku chlorowanie koncentratów w temperaturze 900–1000 °C i odparowanie chlorków, powstających w wyniku reakcji[7]:
- SnO2 + MCl2 + CO = SnCl2 + MO + CO2
- SnO2 + Cl2 + C = SnCl2 + CO2
- SnO2 + 2 HCl + CO = SnCl2 + H2O + CO2
- SnO2 + Cl2 + C = SnCl2 + CO2
Chlorowanie jest selektywne – chlorek żelaza(II) w tych warunkach wchodzi w reakcję:
- 4 SnO2 + 6 FeCl2 = 2 Fe3O4 + 2 SnCl2 + 2 SnCl4
czyli przyspiesza proces uzyskiwania SnCl2.
Prażenie w technologii kwasu siarkowego
Prażenie pirytu (FeS2) i innych siarczków metali, na przykład blendy cynkowej (ZnS), jest procesem umożliwiającym otrzymywanie podstawowego półproduktu w technologii kwasu siarkowego: dwutlenku siarki. Reakcje egzotermiczne przebiegają w uproszczeniu następująco[3][4]:
- piryt
- 4 FeS2 + 11 O2 ——> 8 SO2 + 2 Fe2O3
- 3 FeS2 + 8 O2 ——> 6 SO2 + Fe3O4
- 4 FeS2 + 11 O2 ——> 8 SO2 + 2 Fe2O3
- blenda
- 2 ZnS + 3 O2 ——> 2 SO2 + 2 ZnO
Zakład hutniczy w Trail (1929), w którym opracowano i zastosowano pierwsze konstrukcje pieców mechanicznych, stosowanych później (po modernizacjach) w prażalniach cynku na Górnym Śląsku
Po lewej
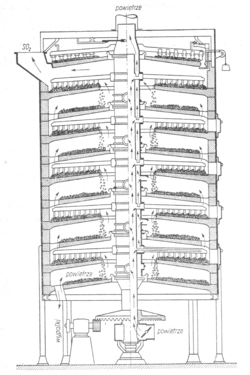
Piec mechaniczny do prażenia pirytów
Przypisy
- ↑ piece, prażak. W: Encyklopedia techniki – Metalurgia. Katowice: Wydawnictwo "Śląsk", 1978, s. 461–492, 527. (pol.).
- ↑ piece. W: "Leksykon naukowo-techniczny z suplementem". T. P-Ż. Warszawa: WNT, 1989, s. 654-657, 728. ISBN 83-204-0969-1.
- ↑ a b c d e f g h Siarczki metali i prażenie siarczków metali. W: Józef Kępiński: Technologia chemiczna nieorganiczna. Warszawa: PWN, 1964, s. 71, 250, 252. (pol.).
- ↑ a b c d e Józef Zawadzki: Technologia chemiczna nieorganiczna, część druga. Warszawa: Ministerstwo Przemysłu i Handlu, Departament Szkolnictwa Zawodowego, 1949, s. 334–367, seria: Biblioteka Techniczna.
- ↑ Palenisko z rusztem ruchomym. [w:] Polytechnik, Polska Sp. z o.o. [on-line]. www.polytechnik.com.pl. [dostęp 2014-03-05]. (pol.).
- ↑ [query=Cassiterite&yt2=Go www.irocks.com - Cassiterite]. [w:] Galleries of Fine Minerals for Sale (zdjęcia minerałów na 'The Arkenstone') [on-line]. old.irocks.com. [dostęp 2015-03-02]. (ang.).
- ↑ Jan Wypartowicz, Andrzej Łędzki, Paweł Drożdż, Ryszard Stachura: Wykład 9: Metalurgia Metali Nieżelaznych > Metalurgia cyny > Prażenie koncentratów. [w:] Prezentacja ppt [on-line]. AGH. s. 14. [dostęp 2014-03-04]. (pol.).
Linki zewnętrzne
- Andrzej Łędzki, Andrzej Michaliszyn, Arkadiusz Klimczyk, „Metalurgia ekstrakcyjna żelaza”. galaxy.uci.agh.edu.pl. [zarchiwizowane z tego adresu (2014-03-05)]. > „Technologia procesu spiekania”, „Spiekanie rud” na: galaxy.uci.agh.edu.pl (AGH), data dostępu: 2015-08-08
Media użyte na tej stronie
(c) Rob Lavinsky, iRocks.com – CC-BY-SA-3.0
Cassiterite
- Locality: Black Hills, South Dakota, USA (Locality at mindat.org)
- Size: miniature, 5.1 x 4.4 x 4.2 cm
- Cassiterite (twinned)
- Tin ore is very limited in the USA. Therefore, it is rare to see large crystals of the primary tin mineral, cassiterite. This one, in quartz, is doubly terminated, lustrous and twinned, with classic, re-entrant faces. The dark gray crystal measures 3.5 cm in length. This is undoubtedly a major American cassiterite and is by far the best I have seen from this locale. However, the combination of form and matrix makes it unique and really quite astonishing for a US piece. Ex. Richard Hauck Collection.
View of a pair of cement kilns with satellite coolers
The Trail Smelter in 1929
Autor: Polimerek (png); user: Marek M (svg), Licencja: CC BY-SA 4.0
A-parowniczka; B-statyw; C-palnik
Piec do prażenia pirytów
Aparat Dwight-Lloyda
Piec zawiesinowy do prażenia blendy cynkowej