Przełącznik molekularny
Przełącznik molekularny (cząsteczkowy) (ang. molecular switch) jest cząsteczką, którą można przełączać pomiędzy dwoma lub więcej termodynamicznie stabilnymi stanami[1].
Przełączanie cząsteczki jest możliwe w odpowiedzi na zmiany:
- pH środowiska
- promieniowania elektromagnetycznego
- temperatury
- prądu lub ładunku elektrycznego
- bezpośrednie wiązanie, kompleksowanie lub inne oddziaływania z cząsteczkami znajdującymi się w otoczeniu przełącznika.
Przełączniki cząsteczkowe są obecnie polem dużego zainteresowania nanotechnologi oraz nanonauk. Przełączniki molekularne pełnią również ważną rolę w biologii. Przykładem jest np. regulacja allosteryczna oraz funkcjonowanie białek motorycznych, będących naturalnymi motorami molekularnymi w komórkach żywych organizmów.
Fotochromowe przełączniki molekularne
Fotochromowe przełączniki molekularne wykorzystują zjawisko fotochromizmu. Związki te zmieniają swoją konfigurację elektronową pod wpływem absorpcji światła o ściśle określonej długości fali. Każdy stan takiej cząsteczki ma maksimum absorpcji, które można określić przy pomocy odpowiedniej metody spektroskopowej. Współcześnie znanych jest wiele przełączników fotochromowych. Są to na przykład pochodne azobenzenu, diaryleteny, (np: stilben), pochodne spiropiranu i wiele innych.
Osobną grupę przełączników fotochromowych stanowią związki chirooptyczne, które posiadają zdolność zmiany swojej konfiguracji absolutnej, a dokładnie przechodzenia z jednego enancjomeru w drugi. Detekcja stanów bistablinych jest tutaj oparta na dichroizmie kołowym, a nie na tradycyjnej spektroskopii świetlne. Przykład takiego związku jest przedstawiony na rysunku poniżej. Jest to zawadzony sterycznie, sprzężony związek heterocykliczny, który pod wpływem naświetlania światłem spolaryzowanym kołowo, przechodzi z jednej formy enacjomerycznej w drugą.
Chirooptyczne przełączniki molekularne, pod wpływem pulsów światła spolaryzowanego kołowo mogą nawet wykonywać ruchy rotacyjne - mogą zatem pełnić rolę motorów molekularnych.[2]:
Przełączniki molekularne typu gospodarz-gość
Pierwszy tego typu przełącznik opisał w 1978 Jean-Pierre Desvergne i Henri Bouas-Laurent[3][4]. Przełącznik ten oparty jest na polieterze do którego przyłączono na obu końcach cząsteczkę antracenu:
Jakkolwiek związek ten nie jest ściśle biorąc bezpośrednio przełączalny, posiada on po naświetleniu ultrafioletem powodującym jego cyklizację, zdolność kompleksowania dwóch kationów metali alkalicznych. Po utworzeniu się kompleksu jest on stabilny również po wyłączeniu źródła światła ultrafioletowego. Pierwotną strukturę związku można przywrócić działając na niego związkiem silniej kompleksującym "złapane w pułapkę" kationy metalu, co powoduje też rozerwanie się pierścienia eteru koronowego.
W 1980 Isamu Yamashita i współpracownicy[5] zsyntetyzowali związek, w którym struktura antracenu jest od razu wbudowana w pierścień eteru koronowego. Związek ten posiadał już bezpośrednią zdolność wiązania kationów metali po naświetleniu i uwalnianiu ich po wyłączeniu źródła światła:
Nie był to jednak wciąż związek, który rzeczywiście miał dwa termodynamicznie stabilne stany.
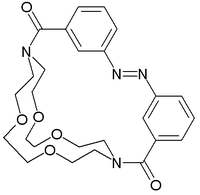
W 1980 r. Seiji Shinkai otrzymał etery koronowe, w których grupy antracenowe zostały zastąpione strukturami azobenzenowymi.[6]. Mechanizm przełączania w tym związku jest oparty na zjawisku zmiany izomerii geometrycznej grup azobenzenowych, polegającej na przejściu z formy trans do cis co wymusza też radykalną zmianę konformacji reszty cząsteczki. W formie trans związek ma powinowactwo do kationów NH4, Li+ i Na+, a w izomerii cis do większych: K+ Rb+. Przełączanie z jednej formy do drugiej jest szybkie i następuje pod wpływem naświetlania ultrafioletem.
Shinkai zastosował ten przełącznik do transportu jonów symulując biochemiczną akcję monenzyny i nigerycyny[7][8]. W układzie dwufazowym jony są pobierane z fazy A w świetle i deponowane w fazie B w ciemności.
Rotaksanowe i katenanowe przełączniki molekularne
Topologiczne przełączniki molekularne są cząsteczkami zbudowanymi z dwóch lub więcej niepowiązanych chemicznie (wiązaniem chemicznym) elementów, zwykle makrycyklicznych. Są to cząsteczki o strukturze katenanu lub rotaksanu. Istnienie dwóch lub więcej termodynamicznie stabilnych stanów układu, zwanych ko-konformerami, wynika ze zmian we wzajemnym, przestrzennym usytuowaniu obu splecionych cząsteczek, czyli izomerii translacyjnej.
W 1991 J. Fraser Stoddart wraz z zespołem[9] opublikował pierwszy w historii rotaksan funkcjonujący jako przełącznik molekularny i zachowujący się jak rodzaj "suwnicy". Jedna z cząsteczek z układu pełni rolę łoża po którym może przesuwać się druga, cykliczna cząsteczka (na niebiesko na rysunku poniżej). W "łożu" znajdują się dwie "stacje końcowe", między którymi może oscylować makrocykliczny fragment układu. W przypadku układu Stoddarta były to ugrupowania bifenylowe (na czerwono na rysunku poniżej) połączone łańcuchem polipeptydu. Stoddart przypuszczał, że kiedy jako stacje włączy się w strukturę "łoża" dwa różne ugrupowania, zdolne na dwa różne sposoby reagować na bodźce zewnętrzne otrzyma się przełącznik molekularny, który będzie mógł pełnić rolę maszyny cząsteczkowej.
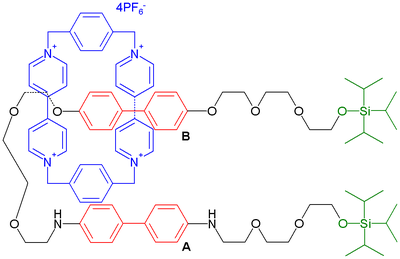
W 1993 r. pionier chemii supramolekularnej Fritz Vögtle opublikował nowy rodzaj przełącznika o strukturze katenanu[10][11]
Jeden z cykli zawiera w swojej strukturze ugrupowanie azobenzenowe, zdolne do zmiany swojej izomerii geometrycznej pod wpływem światła ultrafiletowego oraz dwie "stacje końcowe", którymi są ugrupowania parakwatowe. Drugi cykl to polieter z wbudowanymi dwoma ugrupowaniami fenylowymi, które posiadają silne powinowactwo do parakwatu. Badania NMR wykazały, że gdy ugrupowania azobenzenowe znajdują się w formie trans pierścień polieterowy może swobodnie przemieszczać się wokół swojego partnera. Gdy na układ podziała się światłem ultrafioletowym to ugrupowania azobenzenowe przechodzą w formę cis co blokuje przemieszczanie się pierścienia polieterowego.
W styczniu 2007 Jonathan E. Green wraz z zespołem przedstawili[12] i opatentowali eksperymentalny chip realizujący funkcję pamięci DRAM. Urządzenie to składa się z warstwy 400 krzemowych nanodrutów, pełniących rolę elektrod o średnicy 16 nm rozstawionych w odległościach 33 nm od siebie, która jest skrzyżowana z warstwą 400 elektrod tytanowych o podobnych rozmiarach. Obie warstwy są przedzielone błonką bistablilnego rotaksanu o strukturze przedstawionej poniżej:
Każdy bit w tym urządzeniu jest zapisywany na skrzyżowaniu nanodrutów krzemowego i tytanowego, które są rozdzielone średnio warstwą ok. 100 cząsteczek rotaksanu. Hydrofilowe zakończenie łańcucha polieterowego od lewej strony (R - na rysunku zaznaczony kolorem szarym) zostało tak zaprojektowane aby dawać dobre połączenie z nanodrutem krzemowym specjalnie domieszkowanym na powierzchni fosforem, zaś zakończenie łańcucha od prawej strony (czarne R` na rysunku) jest silnie hydrofobowe i dlatego spontanicznie dąży do nanodrutu tytanowego, dzięki czemu cała cząsteczka jest "rozpięta" między obydwiema elektrodami.
W stanie wyjściowym pierścień zawierający w swojej strukturze parakwat jest umiejscowiony przy ugrupowaniu fulwalenowym (czerwonym). Po przyłożeniu do elektrod różnicy potencjału elektrycznego, fragment fulwalenowy ulega odwracalnej reakcji utlenienia na skutek czego pierścień z parakwatem zostaje wypchnięty i spontanicznie przenosi się na ugrupowanie naftalenowe (na zielono). Gdy po krótkiej chwili fragment fulwalenowy ulega spontanicznej redukcji w układzie pojawia się metastabilny stan, który charakteryzuje zwiększone w stosunku do stanu wyjściowego przewodnictwo elektryczne. Stan ten trwa około godziny, po czym układ ulega relaksacji do stanu wyjściowego. Chip jest zatem przez ten czas w stanie zachowywać zakodowaną w ten sposób informację, bez konieczności zasilania. Jego zaletą w stosunku do obecnie stosowanych pamięci DRAM jest bardzo duża gęstość zapisu - rzędu 1011 bitów na cm2. Używając tej technologii 1,25 GB RAM można zmieścić na 1mm 2 lub inaczej 4,5 TB RAM w typowej wielkości kości DDR2.
Inne przełączniki
- QCAS (quantized conductance atomic switch) - przełącznik zmieniający przewodność, gdzie przełączane są wiązania atomowe. Jeden bit jest kodowany na 1 nm2 przy częstotliwości zmian 1 MHz za pomocą prądu o napięciu 0,6 V.[13]
- Przełączniki wykorzystujące wirusy np. mozaiki tytoniowej.
Przypisy
- ↑ Molecular Machines & Motors (Structure and Bonding) J.-P. Sauvage Ed. ISBN 3540413822
- ↑ Chiroptical Molecular Switches Ben L. Feringa, Richard A. van Delden, Nagatoshi Koumura, and Edzard M. Geertsema Chem. Rev.; 2000; 100(5) pp 1789 - 1816; (Review)
- ↑ Jean-Pierre Desvergne, Henri Bouas-Laurent, Cation complexing photochromic materials involving bisanthracenes linked by a polyether chain. Preparation of a crown-ether by photocycloisomerization, „Journal of the Chemical Society, Chemical Communications” (9), 1978, s. 403-404, DOI: 10.1039/c39780000403, ISSN 0022-4936 (ang.).
- ↑ From Anthracene Photodimerization to Jaw Photochromic Materials and Photocrowns Henri Bouas-Laurent, Alain Castellan and Jean-Pierre Desvergne Pure & Appl. Chem.5 Vol.52, pp.2633—2648. 1980 Link
- ↑ Isamu Yamashita i inni, Synthetic macrocyclic ligands. II. Synthesis of a photochromic crown ether, „Tetrahedron Letters”, 21 (6), 1980, s. 541–544, DOI: 10.1016/s0040-4039(01)85550-7 (ang.).
- ↑ Seiji Shinkai i inni, Photoresponsive crown ethers. 1. Cis-trans isomerism of azobenzene as a tool to enforce conformational changes of crown ethers and polymers, „Journal of the American Chemical Society”, 102 (18), 1980, s. 5860–5865, DOI: 10.1021/ja00538a026, ISSN 0002-7863.
- ↑ Seiji Shinkai i inni, Photoresponsive crown ethers. 2. Photocontrol of ion extraction and ion transport by a bis(crown ether) with a butterfly-like motion, „Journal of the American Chemical Society”, 103 (1), 1981, s. 111–115, DOI: 10.1021/ja00391a021, ISSN 0002-7863.
- ↑ Switch-functionalized systems in biomimetic chemistry Seiji Shinkai Pure & App!. Chem., Vol. 59, No. 3, pp. 425-430, 1987 Link
- ↑ Pier Lucio Anelli, Neil Spencer, J. Fraser Stoddart, A molecular shuttle, „Journal of the American Chemical Society”, 113 (13), 1991, s. 5131–5133, DOI: 10.1021/ja00013a096, ISSN 0002-7863.
- ↑ Photoswitchable Catenanes Fritz Vögtle, Walter Manfred Müller, Ute Müller, Martin Bauer, Kari Rissanen
- ↑ Andrew C. Benniston, Anthony Harriman, A Light-Induced Molecular Shuttle Based on a [2]Rotaxane-Derived Triad, „Angewandte Chemie International Edition in English”, 32 (10), 1993, s. 1459-1461, DOI: 10.1002/anie.199314591.
- ↑ Jonathan E. Green i inni, A 160-kilobit molecular electronic memory patterned at 1011 bits per square centimetre, „Nature”, 445 (7126), 2007, s. 414–417, DOI: 10.1038/nature05462.
- ↑ K. Terabe i inni, Quantized conductance atomic switch, „Nature”, 433 (7021), 2005, s. 47–50, DOI: 10.1038/nature03190.
Media użyte na tej stronie
Synthetic molecular motors: fluorene system.
Mol Switch Stoddart 1994
Dithienylethene acting as a molecular switch.
Molecular Switch Shinkay 1980
Photoswitchable Catenane as described in Fritz Vögtle, Walter Manfred Müller, Ute Müller, Martin Bauer, Kari Rissanen: Photoswitchable Catenanes (1993)