Równanie Clapeyrona (stan gazu doskonałego)
Równanie Clapeyrona, równanie stanu gazu doskonałego – równanie stanu opisujące związek pomiędzy temperaturą, ciśnieniem i objętością gazu doskonałego, a w sposób przybliżony opisujące gazy rzeczywiste. Sformułowane zostało w 1834 roku przez Benoît Clapeyrona[1]. Prawo to można wyrazić wzorem[2][3]:
gdzie[a]:
- – ciśnienie
- – objętość
- – objętość molowa
- – liczba moli gazu, będąca miarą liczby jego cząsteczek; n = v/V
- – temperatura (w kelwinach)
- – uniwersalna stała gazowa: R = NAkB, gdzie: NA – stała Avogadra (liczba Avogadra), kB – stała Boltzmanna, R = 8,314 J/(mol·K)
Równanie to jest wyprowadzane na podstawie założeń:
- gaz składa się z poruszających się cząsteczek;
- cząsteczki zderzają się ze sobą oraz ze ściankami naczynia, w którym się znajdują;
- nie ma oddziaływań międzycząsteczkowych w gazie, z wyjątkiem odpychania w momencie zderzeń cząsteczek;
- objętość (rozmiary) cząsteczek pomija się;
- zderzenia cząsteczek są doskonale sprężyste;

Równanie to, mimo że wyprowadzone w ramach wyidealizowanego modelu, dobrze opisuje większość substancji gazowych w obszarze ciśnień do ok. 100 atmosfer i temperatury do 300–400 °C, oraz w temperaturze trochę większej od temperatury skraplania gazu przy danym ciśnieniu.
Wyprowadzenie
Równanie to można wyprowadzić fenomenologicznie (tj. bez odwoływania się do mikroskopowych właściwości układu). W wyniku wielu eksperymentów przeprowadzonych na gazach głównie w XVIII wieku badacze doszli do wniosku, że można w sposób satysfakcjonujący i wystarczający opisać te przemiany dla 1 mola gazu (n = 1) poprzez podanie 3 zmiennych np. T, p, V. Spośród tych trzech zmiennych tylko dwie są niezależne, wobec czego można traktować np. ciśnienie jako funkcję dwóch pozostałych zmiennych, tj. p = f(T,V). Można zatem zapisać różniczkę zupełną ciśnienia dp jako
Pierwszy człon opisuje proces, w którym gaz zamknięty w stałej objętości jest ogrzewany, czemu towarzyszy zmiana jego ciśnienia. Jako pierwszy taką przemianę opisał Jacques Alexandre Charles (prawo Charles’a) i podał jej równanie w postaci:
skąd wynika
Drugi człon to izotermiczne rozprężanie lub sprężanie gazu opisane przez Boyle’a i Mariotte’a (izotermiczna przemiana Boyle’a-Mariotte’a) wzorem
gdzie l to stała. Z równania tego wynika, że
Otrzymane pochodne cząstkowe podstawmy do wyrażenia na dp
Dzieląc to równanie przez p można rozdzielić zmienne
Po wycałkowaniu
Stałą całkowania C można zapisać przy pomocy innej stałej R
wówczas, ponieważ funkcja ln jest różnowartościowa, a to prowadzi do równania
Rozumowanie można uogólnić na dowolną liczbę moli gazu n. Równanie to stanowi fundamentalny związek między ciśnieniem, temperaturą i liczbą cząstek gazu, z którego wynikają trzy wnioski:
- n moli (taka sama liczba cząstek) gazu, przy danej temperaturze i ciśnieniu panującym w naczyniu zajmuje zawsze taką samą objętość, niezależnie od budowy chemicznej tego gazu (V = nRT/p).
- w danej objętości, przy danym ciśnieniu i temperaturze, znajduje się zawsze taka sama liczba moli cząsteczek gazu, niezależnie od jego budowy chemicznej (n = pV/RT)
- n moli gazu zamkniętych w naczyniu o określonej objętości, przy określonej temperaturze, będzie wywierało na jego ścianki takie samo ciśnienie, niezależnie od tego, jaki to jest gaz (p = nRT/V).
Określenie równanie Clapeyrona nie jest stosowane powszechnie w odniesieniu do tego wzoru – w literaturze anglojęzycznej równanie to znane jest jedynie jako ideal gas law (prawo gazu doskonałego), podobnie jest w większości innych języków. W Rosji równanie to funkcjonuje pod nazwą równania Mendelejewa-Clapeyrona. Jako równanie Clapeyrona określana jest też zależność opisująca przemiany fazowe, m.in. ciecz-gaz. Pod tą nazwą często funkcjonuje też równanie Clausiusa-Clapeyrona.
Rozszerzeniami równania gazu doskonałego, uwzględniającymi objętość cząsteczek gazu oraz przyciąganie cząsteczek, są równanie van der Waalsa oraz wirialne równanie stanu.
Energia gazu
Zgodnie z założeniami kinetycznej teorii gazów zakładaliśmy, że nie ma międzycząsteczkowych oddziaływań pomiędzy cząsteczkami gazu doskonałego. Innymi słowy, jego potencjalna energia wynosi zero. Stąd cała energia posiadana przez gaz jest energią kinetyczną:
Jest to energia kinetyczna jednego mola gazu.
| Energia gazu | Wzór matematyczny |
|---|---|
| energia związana z jednym molem gazu | |
| energia związana z jednym gramem gazu | |
| energia związana z jedną cząsteczką gazu |
Zobacz też
- Przemiany termodynamiczne
- przemiana izobaryczna – (stałe ciśnienie p = const)
- przemiana izotermiczna – (stała temperatura T = const)
- przemiana izochoryczna – (stała objętość V = const)
- przemiana adiabatyczna – (brak wymiany ciepła z otoczeniem Q = 0)
- przemiana politropowa – (pVn = const, gdzie n – wykładnik politropy)
Uwagi
- ↑ Zgodnie z zasadą obowiązującą w termodynamice chemicznej wielkie litery powinny być stosowane do oznaczania wielkości molowych (stąd V – objętość molowa), a litery małe do innych wielkości (stąd v – objętość).
Przypisy
- ↑ Clapeyrona równanie, [w:] Encyklopedia PWN [online] [dostęp 2021-10-08].
- ↑ Encyklopedia techniki. Chemia. Warszawa: WNT, 1965.
- ↑ Antoni Basiński, Bielański Adam, Kazimierz Gumiński i inni: Chemia fizyczna. Wyd. 3. Warszawa: Państwowe Wydawnictwo Naukowe, 1966, s. 297.
Linki zewnętrzne
- applet Java obrazujący działanie przemian gazu doskonałego. walter-fendt.de. [zarchiwizowane z tego adresu (2007-10-23)].
Media użyte na tej stronie
Autor: BlyumJ, Licencja: CC BY-SA 4.0
Molecular collisions within a closed container (the propane tank) are shown (right). The arrows represent the random motions and collisions of these molecules. The pressure and temperature of the gas are directly proportional: as the temperature is increased, the pressure of the propane increases by the same factor. A simple consequence of this proportionality is that on a hot summer day, the propane tank pressure will be elevated, and thus propane tanks must be rated to withstand such increases in pressure.
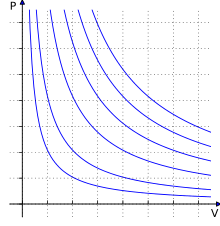
Autor: Krishnavedala, Licencja: CC0
Ideal gas isotherms for one mole of the gas and at temperatures [1, 2, 4, 6, 8, 10]K using the equation . Created using python.


