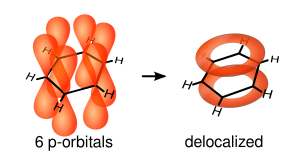Rezonans chemiczny
Rezonans chemiczny (mezomeria) – sposób przedstawiania struktury związków chemicznych i innych indywiduów chemicznych za pomocą tzw. struktur granicznych. Faktyczna struktura cząsteczki jest opisywana przez kombinację liniową tych struktur.
Termin rezonans chemiczny oznacza także samo zjawisko stabilizującego efektu delokalizacji wiązań chemicznych. Rezonans, w świetle mechaniki kwantowej, jest uśrednieniem funkcji falowych opisujących kształt orbitali molekularnych struktur granicznych. Efektem rezonansu jest dodatkowa stabilizacja struktury cząsteczek, która jest ilościowo opisywana przez wielkość zwaną energią rezonansową. Rezonansu nie należy interpretować jako szybkiego cyklicznego przeskoku sąsiadujących wiązań chemicznych. Teoria rezonansu nie dopuszcza możliwości rozdzielenia danej substancji na składniki odpowiadające określonym wzorom[1].
Rezonans chemiczny jest odpowiedzialny za istnienie zjawiska aromatyczności niektórych organicznych związków chemicznych. Występuje on jednak także w wielu związkach niearomatycznych, np. w niektórych dienach. Związki chemiczne, w których występuje zjawisko rezonansu chemicznego, można zapisać w formie tzw. granicznych struktur rezonansowych. W rzeczywistości żadna z tych struktur nie istnieje jako osobne indywiduum, lecz stanowi tylko rodzaj formalnego zapisu, który dopiero łącznie z innymi jest właściwym opisem faktycznej struktury związku. Dla odróżnienia zapisu granicznych struktur rezonansowych od dwóch rzeczywistych związków chemicznych pozostających z sobą w stanie równowagi, stosuje się pojedynczą strzałkę zakończoną z obu stron grotami (↔). Alternatywnie, związki posiadające struktury rezonansowe opisuje się jednym wzorem, w którym występują przerywane linie oznaczające "rozmyte" przez rezonans wiązania o ułamkowej krotności. Dla struktur cyklicznych rysuje się także okręgi lub ich fragmenty oznaczające cały układ wiązań rezonansowych tworzących strukturę aromatyczną:
Z punktu widzenia chemii kwantowej rezonans w cząsteczce benzenu polega na wzajemnym nakładaniu się 6 orbitali p, w wyniku czego powstaje zdelokalizowany orbital molekularny, którego nie da się przedstawić za pomocą tradycyjnych wzorów kreskowych:
Ściśle biorąc, teoria rezonansu w chemii kwantowej pojawia się w teorii wiązań walencyjnych (VB), w której funkcję falową przedstawia się jako kombinację funkcji falowych struktur kanonicznych (rezonansowych), w których wiązania są zlokalizowane.
Zobacz też
- efekt mezomeryczny
Bibliografia
Przypisy
- ↑ I. W: Witold Tomassi: Jony i atomy jako składniki materii. Wyd. Pierwsze. Warszawa: Państwowe Wydawnictwo Naukowe, 1952, s. 37.
Media użyte na tej stronie
Autor: Vladsinger, Licencja: CC BY-SA 3.0
Orbital hybridization in benzene rings.