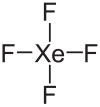Tetrafluorek ksenonu (nazwa Stocka: fluorek ksenonu(IV)), XeF4 – nieorganiczny związek chemiczny z grupy fluorków.
Był pierwszym otrzymanym związkiem chemicznym gazu szlachetnego z dokładnie jednym innym pierwiastkiem. Powstaje w wyniku reakcji ksenonu z fluorem[3]:
- Xe + 2F2 → XeF4
Tworzy bezbarwne kryształy, które sublimują w temperaturze 115,7 °C.
W warunkach normalnych jest stabilny. Pod wpływem wody ulega hydrolizie, w wyniku której w reakcji dysproporcjonowania powstaje m.in. tritlenek ksenonu i ksenon.
- 3XeF4 + 6H2O → XeO3 + 2Xe + 1,5H2O + 12HF
Przypisy
- ↑ a b c d e f CRC Handbook of Chemistry and Physics, David R.D.R. Lide (red.), wyd. 90, Boca Raton: CRC Press, 2009, s. 4-98, ISBN 978-1-4200-9084-0 .
- ↑ a b CRC Handbook of Chemistry and Physics, David R.D.R. Lide (red.), wyd. 90, Boca Raton: CRC Press, 2009, s. 6-53, ISBN 978-1-4200-9084-0 .
- ↑ H.H. Claassen, H. Selig, J.G. Malm. Xenon Tetrafluoride. „J. Am. Chem. Soc.”. 84 (18), s. 3593, 1962. DOI: 10.1021/ja00877a042 (ang.).
Bibliografia
- K. Wieczffiński: Gazy szlachetne: zarys technologii i własności chemiczne. Warszawa: Wydawnictwa Naukowo-Techniczne, 1968.
Linki zewnętrzne