Wanad
| tytan ← wanad → chrom | |||||||||||||||||||||||||||||||||||||||||||
| Wygląd | |||||||||||||||||||||||||||||||||||||||||||
| stalowoszary | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
Widmo emisyjne wanadu | |||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||||||||
| Nazwa, symbol, l.a. | wanad, V, 23 | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grupa, okres, blok | |||||||||||||||||||||||||||||||||||||||||||
| Stopień utlenienia | III, V | ||||||||||||||||||||||||||||||||||||||||||
| Właściwości metaliczne | |||||||||||||||||||||||||||||||||||||||||||
| Właściwości tlenków | |||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa | |||||||||||||||||||||||||||||||||||||||||||
| Stan skupienia | stały | ||||||||||||||||||||||||||||||||||||||||||
| Gęstość | 6110 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||
| Temperatura topnienia | 1910 °C[1] | ||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | 3407 °C[1] | ||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą warunków normalnych (0 °C, 1013,25 hPa) | |||||||||||||||||||||||||||||||||||||||||||
| Ten artykuł od 2011-01 zawiera treści, przy których brakuje odnośników do źródeł. |
Wanad (V, łac. vanadium) – pierwiastek chemiczny z grupy metali przejściowych.
Ma 11 izotopów z przedziału mas 44–55 oraz izomery jądrowe 50m i 52m. Trwały jest tylko izotop 51. W skorupie ziemskiej jest go 160 ppm, w postaci minerałów: patronitu (VS
4), karnotytu i wanadynitu.
Został odkryty po raz pierwszy w 1801 roku przez Andresa Manuela del Rio i później w 1830 roku przez Nilsa Gabriela Sefströma, który nadał mu obecną nazwę na cześć skandynawskiej bogini Vanadis[4].
Ze względu na małe zasoby rud i użyteczność wojskową stanowi jeden z materiałów strategicznych.
Własności
Jest lśniącym, srebrzystym metalem o słabych własnościach mechanicznych. W stanie czystym kowalny i ciągliwy, staje się kruchy powyżej 300 °C.
Tworzy tlenki o stopniach utlenienia od I do V, o różnej strukturze krystalicznej przy tym samym składzie pierwiastkowym. Jest odporny na działanie wody, zasad, rozcieńczonych roztworów kwasów azotowego i siarkowego. Roztwarza się w wodzie królewskiej, kwasie fluorowodorowym i stężonym siarkowym. Wanad ma właściwości paramagnetyczne oraz wykazuje nadprzewodnictwo niskotemperaturowe.
Zastosowanie
- Katalizatory (przede wszystkim V
2O
5 na nośnikach) reakcji utleniania w przemysłowej chemii organicznej, np. utlenianie etylenu do etanolu, oraz w technologii nieorganicznej, np. utlenianie SO
2 do SO
3. - Stosowany jako dodatek do stali poprawiający odporność na ścieranie i pękanie (np. silniki spalinowe, stal narzędziowa)[5].
- Produkcja cermetali.
- Materiał konstrukcyjny reaktorów jądrowych.
- Znacznik promieniotwórczy – sztuczny izotop 48
V otrzymywany w reakcjach 50
Cr(d,α)48
V i 47
Ti(d,n)48
V.
Otrzymywanie
Metody otrzymywania wanadu metalicznego:
- redukcja tlenku V
2O wapniem, - redukcja chlorku VCl
3 magnezem, - redukcja tlenku V
2O
3 węglem, - cieplna dysocjacja jodku VI
3 (najczystszy).
Znaczenie biologiczne
Wanad znajduje się w otoczeniu i pożywieniu człowieka. Przypuszczalnie jest niezbędnym mikroelementem. Ocenia się, że dobowe spożycie wanadu wynosi 10–60 mikrogramów, a zalecane dzienne spożycie 10 mikrogramów. Nie stwierdza się niedoborów wanadu u prawidłowo odżywiających się osób.
Zdarzają się przemysłowe i środowiskowe zatrucia wanadem, najważniejszy efekt to uszkodzenie nerek, podrażnienie błon śluzowych układu oddechowego i pokarmowego.
Suplementacja stosowana przez kulturystów (do 60 miligramów wanadu) nie ma uzasadnienia i może być szkodliwa. Wanad jest pierwiastkiem znajdującym się w centrach aktywnych enzymów przemiany glukozy i innych węglowodanów.
Uwagi
- ↑ Podana wartość stanowi przybliżoną standardową względną masę atomową (ang. abridged standard atomic weight) publikowaną wraz ze standardową względną masą atomową, która wynosi 50,9415 ± 0,0001.
Przypisy
- ↑ a b David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 4-40, ISBN 978-1-4200-9084-0 (ang.).
- ↑ Vanadium (nr 262935) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck KGaA) na obszar Stanów Zjednoczonych. [dostęp 2011-10-05]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Thomas Prohaska i inni, Standard atomic weights of the elements 2021 (IUPAC Technical Report), „Pure and Applied Chemistry”, 94 (5), 2021, s. 573–600, DOI: 10.1515/pac-2019-0603 (ang.).
- ↑ Ignacy Eichstaedt: Księga pierwiastków. Warszawa: Wiedza Powszechna, 1973, s. 193–195. OCLC 839118859.
- ↑ V – Wanad (vanadium) dodatek stopowy, stal narzędziowa, stal szybkotnąca, stale gatunkowe. Alfa-Tech. [dostęp 2015-10-15].
Media użyte na tej stronie
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
Autor:
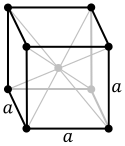
Body-centered cubic crystal structure
Autor:
Alchemist-hp pse-mendelejew.de
Original uploader was Alchemist-hp (www.pse-mendelejew.de) at de.wikipedia, Licencja: CC BY-SA 2.0 deSztabki wanadu o czystości 99,95% przetopione techniką wiązki elektronowej i wytrawione powierzchniowo dla uwidocznienia struktury
Autor: Alchemist-hp (talk) (www.pse-mendelejew.de), Licencja: FAL
A high purity (99.95 %) Vanadium disc, EBM remelted, electrical discharge cut, ground, polished and macro etched. Size ca. 35 mm dia., weight ca. 31.5 g.
Autor: McZusatz (talk), Licencja: CC0
Vanadium spectrum; 400 nm - 700 nm